В случае с мышечной тканью обычные виновники воспаления — микроорганизмы — отходят на второй план. В отличие от кожи и слизистых, постоянно контактирующих с внешней средой, и полостных органов, куда бактерии и вирусы, естественным образом, попадают, мышца — стерильна. Она всегда находится в «футляре»: скелетная мышца покрыта несколькими фасциями, отграничена подкожной жировой клетчаткой; мышечный слой полых органов скрыт под слизистой и подслизистой оболочками, сосудов — под эндотелием, а сердечная мышечная ткань находится под трехслойным эндокардом. Если эти структуры сохранны, к мышце нужен другой подход: патогенный микроорганизм может «достать» до нее разве что тропным токсином, но чаще агрессором становится собственная иммунная система. Сердечная мышца не исключение, и происхождение воспалительного процесса в ней — миокардита — может быть следующим:
- Инфекционным, если микроорганизм обладает тропностью к сердечной ткани и может вызывать иммунную аутоагрессию (например, вирус Коксаки В) или выделяет токсин, поражающий сердечную мышцу (как, например, коринебактерия дифтерии). Миокардит — одно из частых проявлений болезни Лайма. Иногда в миокард «заносит» возбудителей специфических инфекций — туберкулеза или сифилиса, и это приводит к образованию типичных для них гранулем; также возможно поражение сердечной мышцы личинками паразитов при трихинеллезе. Еще более редким случаем является развитие миокардита на фоне ВИЧ-инфекции: фасции и слизистые перестают выполнять свои защитные функции, и даже абсолютно нетипичная для миокарда инфекция (например, грибковая) может распространиться на него гематогенно или контактно из других очагов воспаления в организме; кроме того, повреждающее действие может оказывать и сам ВИЧ. Осталось упомянуть и простейших: специфическое поражение миокарда среди них вызывает Tripanosoma cruzi, возбудитель болезни Чагаса;
- Аутоиммунным и аллергическим; классический пример — системные заболевания соединительной ткани, которые могут затронуть практически любой орган (и не только миокард, если речь идет о сердце, но также и другие его слои). Еще один пример — синдром Лайелла, токсический эпидермальный некролиз, который часто возникает в ответ на введение лекарственных препаратов. В случае развития на фоне синдрома Лайелла миокардита мы не можем точно сказать, является ли его причиной действие самого лекарственного препарата или он возник в результате массивной интоксикации и аутосенсибилизации продуктами распада собственных тканей;
- Токсическим — в ответ на некоторые лекарственные препараты (например, клозапин), интоксикацию тяжелыми металлами (также могут накапливаться в миокарде)
Морфологически воспаление миокарда проявляется фокальным некрозом кардиомиоцитов и интерстициальной инфильтрацией, как правило, лимфоцитарной. Существует особая разновидность миокардита неизвестного происхождения (вероятнее всего аутоиммунного), когда в инфильтрате помимо лимфоцитов присутствуют крупные многоядерные клетки, предположительно макрофаги — гигантоклеточный миокардит. При болезни Чагаса в ткани миокарда можно увидеть трипаносом, а в инфильтрате будут содержаться также и эозинофилы.
Но все же миокард особенная мышца, ее постоянное функционирование жизненно важно для всего организма, и если «нарушение функции», которое сопровождает любое воспаление и тем более некроз, зайдет слишком далеко, миокардит может оказаться смертельным заболеванием. На его фоне может развиться практически любая кардиальная патология, вплоть до серьезных нарушений ритма и острой сердечной недостаточности. Если очаг воспаления затрагивает проводящую систему или структуры, управляющие ритмом, следует ожидать соответствующих нарушений; при диффузном миокардите изменяются эластические свойства всего миокарда, он не может адекватно реагировать на давление в сердечных камерах и поддерживать его — в результате развивается кардиомегалия и сердечная недостаточность.
Но опасность сохраняется и после того, как миновал острый период болезни. Как и после инфаркта миокарда, повреждение какого-то участка воспалительным процессом приводит к ремоделированию миокарда, и после перенесенного миокардита существует риск формирования дилатационной кардиомиопатии (ДКМП), и, следовательно, хронической сердечной недостаточности (ХСН).
Из всех классификаций миокардитов наиболее часто используется клинико-патологическая классификация, предложенная в 1991 г. Е. Либерманом и соавторами:
- Молниеносный миокардит — манифестирует через 2 недели после перенесенного вирусного заболевания, характеризуется выраженной дисфункцией сердца при отсутствии значительной кардиомегалии. Гистологически определяются множественные очаги инфильтрации. Возможно полное выздоровление, но зачастую эта форма миокардита приводит к прогрессирующей сердечной недостаточности и летальному исходу;
- Острый миокардит — манифестирует в более отдаленные сроки с явлений сердечной недостаточности; характеризуется более выраженной кардиомегалией. В исходе, как правило, развивается ДКМП;
- Хронический активный миокардит — начало заболевания трудно отметить; сократительная способность миокарда умеренно снижается, приводя к формированию ХСН. Гистологически наряду с фокусами воспаления отмечают выраженный фиброз. В исходе развивается ДКМП;
- Хронический персистирующий миокардит — относительно благоприятная форма, поскольку значительного снижения фракции выброса и расширения камер сердца не наблюдается;
- Гигантоклеточный миокардит — наоборот, неблагоприятная форма, которая характеризуется рефрактерной прогрессирующей сердечной недостаточностью, нарушениями ритма и проводимости. Имеет характерную гистологическую картину;
- Эозинофильный миокардит — помимо развития умеренной сердечной недостаточности для него характерно образование тромбов в сердечных полостях и, соответственно, тромбоэмболические осложнения.
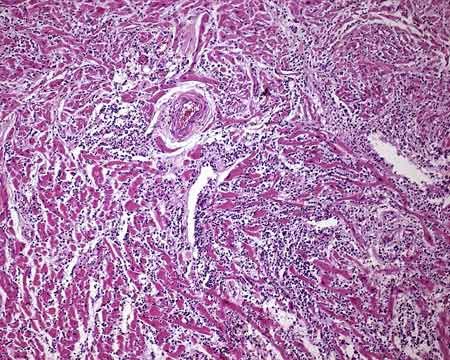
Микроскопическая картина миокардита.
О возможном диагнозе миокардита следует задуматься, если пациент предъявляет следующие жалобы (входят в диагностические критерии при предполагаемом миокардите по рекомендациям ESC 2013):
- острая боль в груди (в области верхушки сердца или слева от грудины, практически постоянная, не зависящая от нагрузки и не купирующаяся нитроглицерином);
- появление впервые или ухудшение имевшихся симптомов сердечной недостаточности за период менее 3 месяцев (появление или усугубление одышки в покое, утомляемости, признаков застоя по малому или большому кругу кровообращения: положение ортопноэ, приступы удушья по ночам
- признаки левожелудочковой недостаточности; отеки на ногах, боли в правом подреберье — признаки правожелудочковой недостаточности);
- синкопе, приступы сердцебиения, предотвращенная внезапная сердечная смерть;
- кардиогенный шок неизвестной этиологии.
Все остальные анамнестические и клинические признаки также рассмотрены в рекомендациях, но служат дополнительными и такой диагностической ценности не несут.
Кроме различных по выраженности признаков сердечной недостаточности при физикальном осмотре больного врач может обнаружить:
- лихорадку, как правило, субфебрильную;
- приглушенные, вплоть до полного отсутствия, тоны сердца; протодиастолический ритм галопа, не соответствующая лихорадке тахикардия или аритмия, функциональный систолический шум на верхушке (расширено сердце, растянуто кольцо митрального клапана, отсюда относительная его недостаточность);
- расширение границ абсолютной и относительной сердечной тупости;
- снижение систолического и пульсового артериального давления, соответствующие нарушению ритма изменения пульса.
Ценными являются анамнестические сведения о перенесенной вирусной инфекции, сопутствующих аллергических или аутоиммунных заболеваниях, наличии семейного анамнеза миокардитов и ДКМП, а также нахождении женщины в момент заболевания в перипартальном периоде (послеродовом).
Из дополнительных методов обследования наиболее значимы (входят в клинические критерии ESC 2013) результаты следующих:
ЭКГ. Более информативно исследование ЭКГ в динамике. Наиболее часто отмечаются следующие изменения:
- депрессия или подъем сегмента RS-T как признак выраженных ишемических и метаболических нарушений в субэндо- и субэпикардиальных слоях. Выраженность не всегда коррелирует с тяжестью поражения миокарда;
- изменения комплекса QRS: низкий вольтаж, появление патологического зубца Q;
- внутрижелудочковые и АВ-блокады, коррелирующие с тяжестью процесса. АВ блокады II–III степени и блокады ножек пучка Гиса свидетельствуют о диффузном поражении миокарда и неблагоприятном прогнозе;
- различные нарушения ритма вплоть до фибрилляции желудочков.
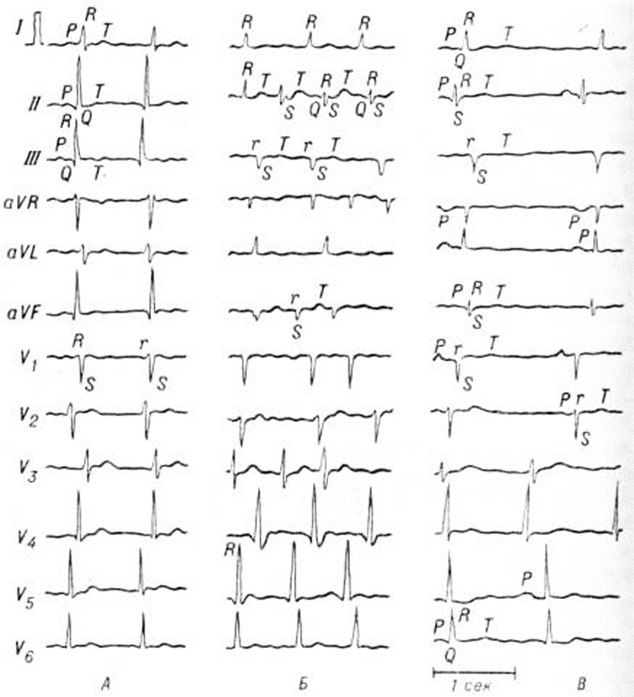
Электрокардиограмма в 12 общепринятых отведениях: А — здорового человека, Б и В — больного гриппозным миокардитом;
Б — ЭКГ на 3-й день болезни: мерцательная тахиаритмия с частотой сердечных сокращений около 100 в 1 минуту (зубец Р отсутствует), на фоне учащения сердечных сокращений (отведение II) появляется функциональная внутрижелудочковая блокада с аберрантным проведением импульса, в связи с чем все комплексы QRS имеют разную форму; имеются признаки блокады передне-верхней ветви левой ножки пучка Гиса — низкие зубцы R (r) и глубокие S в отведениях III и aVF;
В — ЭКГ на 17-й день болезни: восстановился синусовый ритм, перед всеми желудочковыми комплексами QRS виден зубец Р; интервал Р-Q равен 0,2 секунд Выраженная синусовая брадикардия и синусовая аритмия (частота сердечных сокращений колеблется от 34 до 54 в 1 минуту) свидетельствуют о снижении функции синусового узла.
ЭхоКГ — используется для оценки степени нарушения сократительной функции миокарда. В пользу диагноза миокардита говорят:
- увеличение конечно-диастолического и конечно-систолического объема левого желудочка (его дилатация), при этом стенка может быть утолщена за счет интерстициального отека; реже наблюдают дисфункцию правого желудочка;
- фракция выброса ниже 50 %; уменьшение ниже 30 % — плохой прогностический признак;
- относительная недостаточность митрального клапана, митральная регургитация и увеличение объема левого предсердия;
- внутрисердечные тромбы;
- сепарация листков перикарда и жидкость в околосердечной сумке при присоединении перикардита.
МРТ — не рекомендуется пациентам в жизнеугрожающем состоянии, у остальных может использоваться для верификации диагноза. Используются МРТ-критерии диагностики миокардита (Lake Louise Criteria), наличие 2-х из нижеперечисленных признаков позволяет поставить диагноз.
- Локальное или диффузное повышение интенсивности сигнала на Т2-взвешенных изображениях;
- Повышение соотношения между интенсивностью сигнала миокарда и скелетной мускулатурой в раннюю фазу контрастирования;
- Наличие как минимум одного участка накопления контрастного препарата в отсроченную фазу, что может свидетельствовать о некротических или фибротических изменениях сердечной мышцы.
Коронароангиография (КАГ) — рекомендуется всем пациентам с подозрением на миокардит для исключения ишемической природы сердечных симптомов.
Эндомиокардиальная биопсия (ЭМБ) — золотой стандарт диагностики миокардита. Показана всем пациентам, у которых на основании вышеприведенных значимых клинических признаков подозревают миокардит. Оценка результатов проводится на основании Далласских морфологических критериев:
- Диагноз острого миокардита ставится при наличии ≥ 14 лейкоцитов/мм² миокарда в сочетании с признаками некроза и дегенерации;
- Хронический миокардит характеризуется ≥ 14 лейкоцитов/мм², отсутствием признаков некроза и дегенерации при наличии фиброза;
- Отсутствие миокардита подтверждается, если количество инфильтрирующих миокард клеток < 14 лейкоцитов /мм². Эти 14 лейкоцитов по данным иммуногистохимического анализа должны включать до 4 моноцитов/мм² и ≥ 7 клеток/мм² CD3+ Т-лимфоцитов. Исследование дополняют ПЦР-анализом для определения этиологии миокардита.
Маркеры цитолиза. Из биохимических методов в критерии диагностики вошло определение сердечных тропонинов T и I, хотя их нормальное значение и не исключает диагноз миокардита.
Но есть и другие исследования, которые часто применяются в клинике и могут быть информативны:
- Определение неспецифических маркеров воспаления (повышение СОЭ, содержания С-реактивного белка, фибриногена, серомукоида и т. п., лейкоцитоз, сдвиг лейкоцитарной формулы влево) — как правило, отсутствуют при хронических и подострых миокардитах;
- Иммунологические исследования с определением титра противокардиальных антител — больше подходят для определения прогноза и показаний к плазмаферезу; Они часто обнаруживаются при серодиагностике вирусных инфекций и в отсутствие миокардита и плохо коррелируют с результатами ЭМБ, являющейся золотым стандартом;
- Маркеры сердечной недостаточности: мозговой натрийуретический пептид и его N-терминальный фрагмент;
- Рентгенография грудной клетки часто проводится пациентам с кардиальной симптоматикой. При миокардите будет наблюдаться кардиомегалия, возможны рентгенологические признаки застоя в легких и плеврального выпота — то есть картина сердечной недостаточности, не специфичную для миокардита;
- Радионуклидная диагностика позволяет визуализировать в миокарде очаги воспаления и некроза, особенно при использовании моноклональных антител к актомиозину, меченых индием. В настоящее время этот метод считают более подходящим для диагностики саркоидоза.
Лечение
Даже если пациент с миокардитом не предъявляет жалоб, острая сердечная недостаточность или жизнеугрожающее расстройство ритма могут развиться в любой момент, поэтому всех пациентов с диагнозом миокардит следует госпитализировать.
Помощь при таких неотложных состояниях, если они все же развиваются — первое направление в терапии миокардитов; второе направлено на борьбу с их причиной и состоит в борьбе с вирусом-возбудителем и модуляции активности иммунной системы.
Из немедикаментозных мер применяются классические подходы в лечении сердечной недостаточности и аритмий.
В острый период и в последующие 6 месяцев больным рекомендуют ограничить физическую нагрузку, а в период стабилизации симптомов сердечной недостаточности после перенесенного миокардита она, наоборот, полезна.
Также следует соблюдать диету с ограничением приема соли до 2–3 г/сут и жидкости до 1–1,2 л/сут, повышенным содержанием ионов калия и магния.
Поскольку опасность развития аритмий резко снижается после разрешения острой фазы, таким больным нецелесообразно ставить постоянные устройства для поддержания ритма.
- пациентам с брадикардией или блокадой, провоцирующими фибрилляцию желудочков, в острый период миокардита рекомендуют постановку временного электрокардиостимулятора;
- пациентам с тяжелой дисфункцией или электрической нестабильностью желудочков рекомендуют носимые дефибрилляторы; если после разрешения острой фазы необходимость в них не исчезает, ставят постоянный имплантируемый кардиовертер-дефибриллятор;
- исключение в последней группе составляют пациенты с гигантоклеточным миокардитом — им кардиовертер-дефибриллятор имплантируют сразу. Такой вариант следует рассмотреть и при наличии персистирующих воспалительных инфильтратов/МРТ признаков фиброза в миокарде.
При фульминантном миокардите пациентам может потребоваться гемодинамическая поддержка вплоть до искусственного кровообращения.
Медикаментозная терапия включает лечение сердечной недостаточности по существующим для нее стандартам. Назначают:
- Ингибиторы АПФ или блокаторы рецепторов ангиотензина — при раннем назначении уменьшают степень ремоделирования миокарда и риск развития ДКМП;
- Бета-блокаторы;
- Диуретики (предпочтителен торасемид);
- Антагонисты минералокортикоидных рецепторов — рекомендованы только при значительном снижении фракции выброса и выраженной сердечной недостаточности.
Из всей иммуномодулирующей терапии при миокардите однозначно рекомендованы только иммуносупрессоры. Иммуносупрессивная терапия проводится после исключения активной инфекции в миокарде по данным ПЦР. Используют:
- при эозинофильном и токсическом миокардите — монотерапию стероидами (метилпреднизолон 1 мг/кг/сут);
- при других формах, в том числе при лимфоцитарном миокардите — двойная терапия: стероиды + иммуносупрессоры (азатиоприн — 2 мг/кг/сут, циклоспорин — в зависимости от концентрации в крови);
- при гигантоклеточном миокардите — двойная (метилпреднизолон + циклоспорин) или тройная (метилпреднизолон + циклоспорин + азатиоприн) терапия.
Назначение иммуноглобулинов, нестероидных противовоспалительных препаратов и иммуносорбции не рекомендуется.
Из противовирусных препаратов рекомендуются только интерфероны бета-1b при доказанной энтеровирусной природе заболевания.





