Невролог-исследователь нашел признаки подлога в десятках статей, посвященных болезни Альцгеймера, что теперь ставит под сомнение господствующую теорию развития этой болезни.
В августе 2021 года Мэтью Шрагу, нейробиологу и врачу из университета Вандербильта, позвонили, после чего он буквально погрузился в водоворот событий. Коллега хотел связать его с адвокатом, расследующим дело об экспериментальном препарате для лечения болезни Альцгеймера под названием Симуфилам. Представители компании-разработчика препарата («Cassava Sciences») заявили, что он способствует улучшению когнитивных функций, отчасти за счет восстановления белка, который может блокировать отложение липкого белка β-амилоида (Aβ) в мозге (это, согласно доминирующей ныне концепции, является ключевым гистологическим признаком болезни Альцгеймера). Клиенты адвоката, два видных нейробиолога, которые при этом также были «продавцами на понижение» (в случае падения акций компании они получили бы прибыль), полагали, что некоторые исследования Симуфилама могли оказаться искусными подделками (согласно петиции, поданной позже от их имени в Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США [U.S. Food and Drug Administration, FDA]).
37-летний Шраг — тихий, с вечно растрепанными волосами, преподаватель-стажер, уже приобрел определенную известность, подвергнув публичной критике противоречивое одобрение FDA препарата Адухелм (действующего против Aβ). Также выводы его собственного исследования противоречили некоторым утверждениям «Cassava Sciences». Он опасался, что добровольцы в продолжающихся испытаниях Симуфилама испытывают определенные побочные эффекты без шансов на развитие полезных эффектов.
Поэтому Шраг пустил в ход все свои технические способности и знания в области медицины, чтобы изучить опубликованные изображения, полученные по итогам исследований препарата, а также научную основу тех процессов, на которые нацелен препарат. За это адвокат заплатил ему 18 000 долларов. Шрагу удалось выявить явно измененные или продублированные изображения в десятках статей в разных изданиях. Адвокат сообщил о многочисленных открытиях, отраженных в петиции FDA, а Шраг отправил эти сведения в Национальный институт здравоохранения (NIH), представители которого вложили в работу десятки миллионов долларов.
Но расследование Шрага втянуло его в изучение еще одного случая противоправного поведения, а это уже привело к выводам, представляющим угрозу одному из самых цитируемых исследований болезни Альцгеймера в этом столетии и многочисленным экспериментам, основанным на нем.
Первым автором этого влиятельного исследования, опубликованного в журнале «Nature» в 2006 году, был подающий надежды нейробиолог Сильвен Лесне из университета Миннесоты (UMN), что в Миннеаполисе и Сент-Поле. Работа Лесне поддерживает ключевой элемент доминирующей, но спорной гипотезы болезни Альцгеймера — гипотезы амилоида, согласно которой скопления Aβ (т. н. бляшки) в тканях головного мозга являются основной причиной недуга, от которого страдают десятки миллионов людей во всем мире. Что еще больше выглядело как неопровержимое доказательство теории и могло привести к разработке возможных лекарственных средств, так это то, что Лесне с соавторами обнаружили разновидность Aβ у крыс и, казалось, доказали, что он вызывает деменцию у этих животных. Если сомнения Шрага верны, результаты работы Лесне оказались подробно разработанной мистификацией.
Шраг, который до этой статьи публично не позиционировал себя как разоблачителя, в своей критике работы Лесне и исследований, проводимых под эгидой «Cassava Sciences», избегает таких выражений, как «мошенничество», и не утверждает, что доказал факт противоправного поведения. Для доказательства подобного потребуется доступ к исходным, неопубликованным изображениям и даже к необработанным числовым данным. По словам самого Шрага, он сосредоточен на содержании опубликованных изображений и описывает их лишь как тревожные сигналы, а не как окончательные выводы. «Данные должны говорить сами за себя».
Шестимесячное расследование, проведенное «Science», убедительно подтвердило подозрения Шрага и подняло новые вопросы об исследованиях Лесне. Ведущий независимый аналитик изображений в исследованиях и несколько ведущих ученых, занимающихся проблемой болезни Альцгеймера, в том числе Джордж Перри из Техасского университета в Сан-Антонио и Джон Форсайт из Калифорнийского университета в Сан-Франциско (UCSF), проанализировали результаты Шрага по запросу «Science». Ученые согласились с его выводами, согласно которым под сомнение ставится несколько сотен изображений, в том числе и более 70 — из статей Лесне. А Донна Уилкок, эксперт по болезни Альцгеймера из университета Кентукки, сообщает, что некоторые из этих изображений выглядят как примеры «беззастенчивых» подделок.
Как заявляет Элизабет Бик, молекулярный биолог и известный консультант по судебно-медицинским изображениям, похоже, что авторы составили изображения в статьях путем компиляции фрагментов фотографий из разных экспериментов. Она продолжает, что полученные экспериментальные результаты могли не соответствовать желаемым, и эти данные могли быть изменены в пользу лучшего соответствия гипотезе.
В начале 2022 года Шраг высказал свои сомнения перед NIH и представителями изданий, в том числе и «Nature»; в период с 11 по 17 июля в двух изданиях, включая «Nature», были опубликованы соответствующие предупреждения по поводу статей Лесне. Работа Шрага, выполненная независимо от Вандербильтского университета и медицинского центра при нем, подразумевает, что миллионы долларов из федерального бюджета могли быть потрачены не по назначению, — а соответственно, и работы, являвшиеся концептуальным продолжением. Некоторые эксперты по болезни Альцгеймера и вовсе подозревают, что исследования Лесне на последующие 16 лет направили в неверное русло работы по болезни Альцгеймера.
Томас Зюдхоф, лауреат Нобелевской премии, нейробиолог из Стэнфордского университета и эксперт по болезни Альцгеймера, сообщает, что непосредственный и очевидный ущерб — это финансирование впустую от NIH и пустые умозаключения в этой области, ведь люди используют эти результаты как отправную точку для своих собственных экспериментов.
Сам Лесне не ответил на запросы с просьбами прокомментировать ситуацию. Представитель UMN сообщил, что университет находится в процессе рассмотрения жалоб на его работу.
По мнению Шрага, два спорных направления исследований Aβ поднимают масштабные вопросы о научной честности в сфере понимания и лечения болезни Альцгеймера. Он считает, что некоторые сторонники гипотезы амилоида слишком слепо верят в правильность работы, что, похоже, свидетельствует о пристрастном отношении к ней. Даже если противоправные действия случаются редко, ложные идеи, находящиеся в ключевых узлах существующей научной концептуальной картины, искажают последнюю.
В скромном кабинете Шрага, в нескольких шагах от гудящего холодильника, находится старинный микроскоп — дань уважения отцам-основателям, которые применяли кропотливые лабораторные методы к постижению бесконечных загадок медицины. Небольшая табличка на его столе гласит: «Во всем можно разобраться».
До сих пор болезнь Альцгеймера была исключением. Но опыт Шрага позволил ему найти выход из существующих противоречий в этой области. Отец Шрага — из семьи-представителей религиозной группы меннонитов, известных своей философией пацифизма, однако он пошел в армию. Семья переезжала из Аризоны в Германию, затем в Англию, прежде чем поселиться в Давенпорте, крошечном городке на востоке штата Вашингтон. После увольнения из ВВС отец Шрага начал работать медбратом в доме престарелых. Подростком Шраг навещал там пациентов с деменцией. Он вспоминает, как удивлялся тогда поведению пациентов. Тем не менее, он отмечает, что для него это был полезный опыт «видеть, как люди борются с такими тяжелыми симптомами».
Получив домашнее образование благодаря своей маме, в 16 лет Шраг, как и многие прилежные ученики, поступил в местный колледж. Там же он познакомился и со своей будущей женой Сарой. Сейчас они живут на небольшом ранчо возле Нэшвилла, воспитывают двух маленьких детей и содержат на ферме трех стареющих лошадей, за которыми с детства ухаживала Сара.
Готовясь к поступлению в медицинскую школу в университете Северной Дакоты, Шраг проводил долгие часы в лаборатории нейрофармакологии, старательно постигая основы науки. Он многократно выполнял эксперименты, совершенствуя свои навыки. К числу последних относился и метод идентификации белков, называемый вестерн-блоттингом. Его принцип заключается в пропускании образцов тканей, богатых белком, сквозь электрическое поле, через толщу специального геля, который выполняет роль сита для разделения молекул по размеру. Отдельные белки, помеченные и подсвеченные флуоресцентными антителами, выглядят как упорядоченные полосы.
В первой публикации Шрага, выпущенной в 2006 году, обсуждалось, как кормление кроликов продуктами, богатыми холестерином, приводило к увеличению бляшек Aβ и отложению железа в одной части мозга. Вскоре после этого, когда он уже выпустился из медицинской школы и был аспирантом в университета Лома Линда, другой исследовательской группе удалось обнаружить связь между болезнью Альцгеймера и метаболизмом железа. Воодушевившись, Шраг приложил все усилия, чтобы подтвердить существование такой связи у людей, — и потерпел неудачу. Этот опыт стал для Шрага новым витком в изучении болезни Альцгеймера. Как оказалось, в случае с этой загадочной патологией даже тщательно продуманные эксперименты, проведенные добросовестно, могут не воспроизвестись, что обернется тупиковыми ситуациями и неожиданными неудачами.
Самой же большой загадкой является главная отличительная особенность болезни: те самые бляшки и другие белковые отложения, которые немецкий патологоанатом Алоис Альцгеймер впервые увидел в 1906 году в тканях мозга умершего пациента с деменцией. В 1984 году в качестве основного компонента бляшки был определен Aβ. А в 1991 году исследователям удалось зафиксировать мутации в гене белка-предшественника, из которого происходит амилоид (на материале семейной формы болезни Альцгеймера). Многим ученым казалось очевидным, что накопление Aβ запускает каскад повреждений нейронов, которые приводят к деменции. Соответственно, наиболее очевидной стратегией терапии должно было стать то, как остановить отложение амилоида.
Однако сотни клинических испытаний препаратов, нацеленных на амилоид, принесли крайне мало надежд на успех; разве что только Адухелм (как пишет автор статьи, «крайне заурядный препарат» — прим. перев.) был одобрен FDA. Тем не менее, в исследованиях и разработке лекарств Aβ по-прежнему доминирует в качестве основной цели медикаментозного воздействия. В этом финансовом году NIH было потрачено порядка 1,6 миллиарда долларов на проекты, в которых так или иначе упоминается воздействие на отложение амилоида, а это около половины от общего объема финансирования исследований болезни Альцгеймера. Ученые-сторонники других потенциальных причин развития болезни Альцгеймера, как например, дисфункция иммунной системы или же воспаление, выражают недовольство тем, что эти гипотезы отодвинуты на второй план «амилоидной мафией». Форсайт вообще сравнивает амилоидную гипотезу с Птолемеевской моделью Солнечной системы, согласно которой Солнце и планеты вращаются вокруг Земли (это т. н. геоцентрическая система мира, одним из ведущих апологетов которой был античный естествоиспытатель II в. н. э. Клавдий Птолемей — прим. перев.).
К 2006 году, к столетию грандиозного открытия Алоиса Альцгеймера, все более растущая группа скептиков уже открыто задавалась вопросом о необходимости перезагрузки в этой области. А затем эту брешь заполнила невероятная статья в «Nature».
Работа, стоящая за этой публикацией, протекала в лаборатории нейробиолога и врача из UMN Карен Эш, которая уже сделала ряд выдающихся открытий. Еще будучи резидентом UCSF, она участвовала в новаторской работе лауреата Нобелевской премии Стэнли Прузинера, посвященной прионам — белкам-инфекционным патогенам, вызывающим редкие неврологические расстройства. В середине 1990-х ей удалось вывести трансгенную мышь, у которой синтезировался человеческий Aβ, образовывавший бляшки в мозге животного. У мыши также проявлялись симптомы, сходные со слабоумием. Это и была так полюбившаяся исследователям модель болезни Альцгеймера.
К началу 2000-х представление о «токсичных олигомерах», разновидности Aβ, которые способны растворяться в некоторых биологических жидкостях организма, заняло место главной причины развития болезни Альцгеймера. Потенциально эти олигомеры были даже более патогенными, чем нерастворимые бляшки. Оказалось, что амилоидные олигомеры были связаны с нарушением межклеточной коммуникации между нейронами in vitro и у животных, а результаты аутопсий людей свидетельствовали о более высоком содержании олигомеров в мозге людей с болезнью Альцгеймера, чем когнитивно здоровых людей. Однако никому не удалось доказать, что хотя бы один из известных олигомеров является непосредственной причиной снижения когнитивных функций.
В мозге трансгенных мышей, выведенных Эш, команда ученых из UMN обнаружила ранее неизвестный вид олигомера, получивший название Aβ*56 по причине его относительно большой молекулярной массы в сравнении с другими олигомерами. Группе удалось выделить Aβ*56 и ввести его молодым крысам. Способность крыс вспоминать простую, ранее полученную информацию, например, местонахождение скрытой педальки в лабиринте, резко снизилась. Первым автором статьи 2006 года, которого иногда называют первооткрывателем Aβ*56, был именно Лесне, молодой ученый, которого Эш наняла сразу после получения степени Ph.D. по программе университета Кан-Нормандия во Франции.
На своем веб-сайте Эш позиционировала Aβ*56 как «первое когда-либо идентифицированное вещество из тканей мозга в исследованиях болезни Альцгеймера, которое достоверно приводит к ухудшению памяти». В сопутствующей редакционной колонке в «Nature» Aβ*56 был назван «главным подозреваемым» в развитии болезни Альцгеймера. В Alzforum, популярном онлайн-ресурсе по этой области, репортаж был озаглавлен «Aβ Star is Born?» («Звезда Aβ взошла?»). Менее чем через две недели после публикации статьи Эш получила престижную Потамкинскую премию в области неврологии, в том числе и за работу, приведшую к открытию Aβ*56.
Согласно базе данных Web of Science, та статья в «Nature» была процитирована примерно в 2300 научных статьях — больше, чем во всех, кроме четырех, основных работах, посвященных болезни Альцгеймера, опубликованных с 2006 года. С тех пор ежегодная поддержка исследований, где фигурировали бы термины «амилоид», «олигомер» и «болезнь Альцгеймера», со стороны NIH выросла почти с нуля до 287 миллионов долларов к 2021 году. Работы Лесне и Эш стали той искрой, что зажгла множество новых исследований в этой области, как отмечают эксперты.
По словам Зюдхоф, та статья придала «новый импульс» гипотезам об амилоиде и токсических олигомерах, что было особенно актуально в свете «конфликта» с другими гипотезами (и, соответственно, сомнениями). Сторонникам же гипотезы амилоида это понравилось, потому что казалось, что это независимое подтверждение их предложениям, выдвигавшимся в течение длительного времени.
По словам Уилкок, это было действительно важное открытие, которое, казалось, открыло всю картину болезни. Отчасти это произошло из-за безукоризненного разрешения на работу Эш. Именно это и побудило многих других исследователей отправиться на поиски более тяжелых форм олигомеров.
Когда звезда Эш загорелась ярче, взошла звезда Лесне. Он присоединился к команде UMN со своей собственной лабораторией, финансируемой NIH, в 2009 году. Исследование Aβ*56 оставалось основным направлением работы. Меган Ларсон, которая работала младшим научным сотрудником у Лесне, а ныне является руководителем производства в компании-поставщике биологической продукции «Bio-Techne», называет его страстным, трудолюбивым и харизматичным сотрудником. Ларсон продолжает, что ей и сотрудникам лаборатории доводилось часто проводить эксперименты и вестерн-блоттинг, однако в их совместных статьях Лесне готовил для публикации все изображения.
В 2020 году он стал руководителем аспирантской программы UMN по нейробиологии, а в мае 2021 года, через четыре месяца после того, как Шраг поделился своими соображениями-опасениями с NIH, Лесне получил от агентства желанный грант R01 с поддержкой до пяти лет. Инспектор по программе грантов NIH Остин Янг — соавтор той статьи в «Nature» 2006 года — отказался от комментариев.
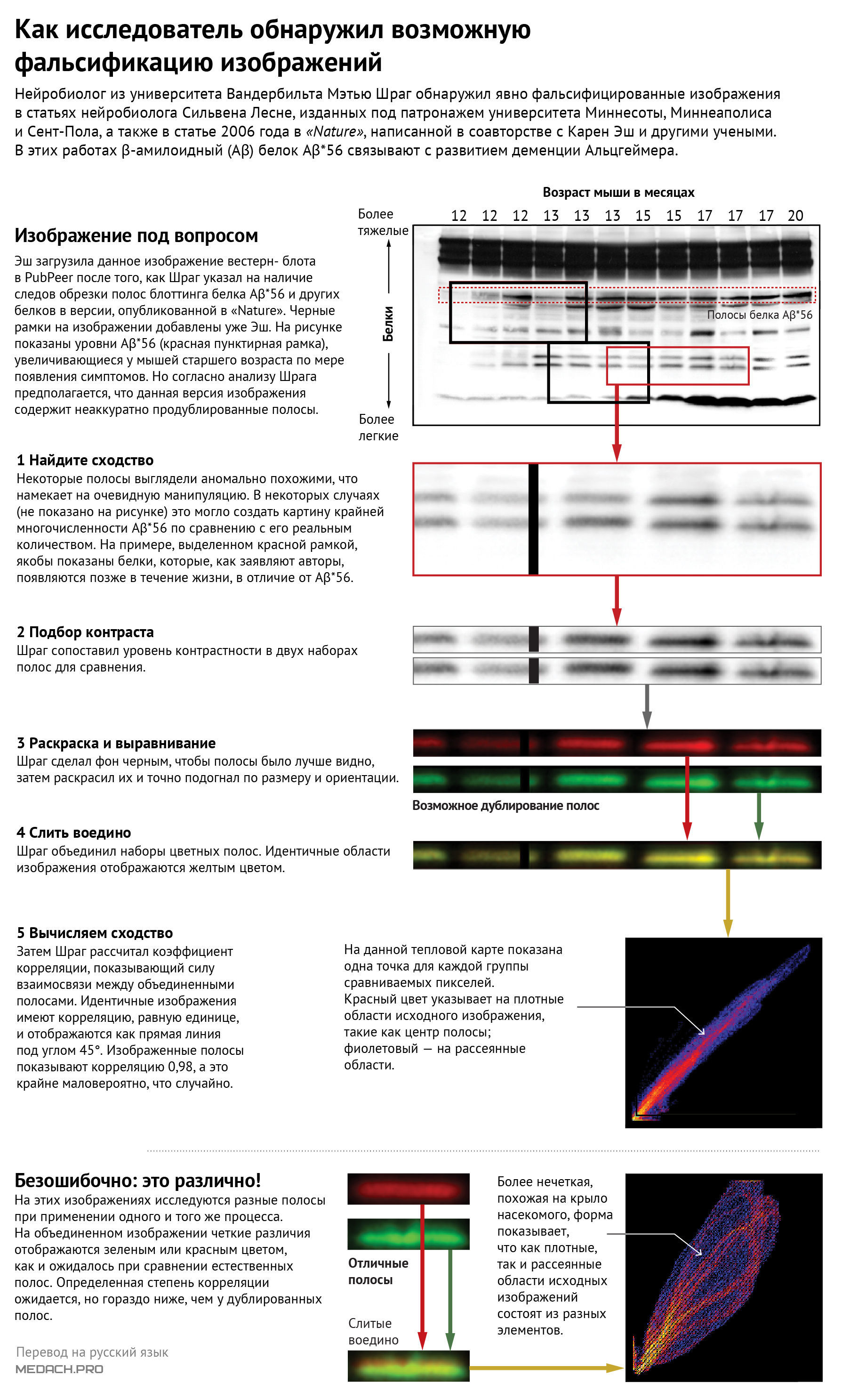
В декабре 2021 года Шраг зашел на PubPeer — веб-сайт, на котором ученые отмечают возможные ошибки в опубликованных статьях. Многие посты на сайте исходят от технарей, которые проводят деконструирование результатов вестерн-блоттинга по ключевым меткам, указывающим на то, что полосы, отображающие белки, могли быть удалены или вставлены туда, где они быть не должны. Такие манипуляции могут привести к ложному предположению о присутствии белка или изменении его концентрации, при которой данный белок можно выявить. Шраг же, по-прежнему сосредоточенный на работах компании «Cassava Sciences», вел поиск примеров, которые могли бы способствовать развитию его собственного расследования.
В поиске сайта PubPeer по запросу «болезнь Альцгеймера» внимание Шрага привлекли сообщения о статьях в «Journal of Neuroscience». В этих статьях ставится под сомнение подлинность результатов вестерн-блоттинга, используемых для дифференцировки Aβ и ему подобных белков в тканях мозга мыши. Было похоже на то, что несколько полос были продублированы. Используя программное обеспечение, Шраг подтвердил комментарии на PubPeer и обнаружил аналогичные проблемы с другими результатами блоттинга в тех же статьях. Он также обнаружил несколько фоновых блотов, которые, похоже, были неправильно продублированы.
В трех статьях Лесне, о котором Шраг никогда не слышал, указан в качестве первого или старшего автора. Шраг быстро выявил, что еще одна статья Лесне также привлекла внимание на PubPeer, и расширил свой поиск до всех статей этого автора, которые там не были отмечены как проблемные. По его словам, исследование продвигалось своим чередом по мере того, как возникали другие очевидные проблемы.
Шраг поясняет, что в данной области очень многое крайне трудно воспроизвести, поэтому понимание того, когда данные могут оказаться ненадежными, является огромным преимуществом. Отчасти это произойдет при воспроизведении полученных результатов в самой лаборатории. Но если это можно сделать более простыми и быстрыми способами, такими как анализ изображений, то лучше воспользоваться этим путем. В конце концов, Шраг наткнулся на ту самую судьбоносную статью в «Nature», ставшую основой для многих других. В ней, похоже, также содержалось несколько поддельных изображений.
«Science» попросила двух независимых аналитиков изображений — Элизабет Бик и Яну Кристофер — проанализировать выводы Шрага об этой и других работах Лесне. По их заявлениям, некоторые предполагаемые манипуляции могут быть лишь цифровыми артефактами, которые могут возникать непреднамеренно во время обработки изображений, и Шраг допускает возможность такого. Но, тем не менее, Бик находит свои выводы убедительными. Кристофер соглашается с тем, что многие продублированные изображения и некоторые пометки указывают на вырезанные и вставленные изображения вестерн-блотов (которые Шраг определил как проблемные). Также она выявила еще несколько сомнительных блотов, которые Шраг пропустил.
В течение 16 лет после знаменательной статьи Лесне и Эш было опубликовано множество статей об этом звездном олигомере. Тем не менее, лишь несколько других исследовательских групп сообщали об обнаружении Aβ*56.
Ссылаясь на текущую проверку UMN работы Лесне, Эш отказалась давать интервью или отвечать по электронной почте на вопросы от представителей «Science», которые она назвала «отрезвляющими». Но она написала, что все еще верит в Aβ*56, отметив свою текущую работу по изучению структуры олигомеров Aβ. Она заявила, что у ее команды есть многообещающие результаты, и она по-прежнему в восторге от этой работы и может объяснить, почему терапия Aβ все еще может оказаться эффективной, несмотря на недавние неудачи в отношении амилоидных бляшек.
Но еще до расследования Шрага разрозненные доказательства того, что Aβ*56 играет ведущую роль в развитии болезни Альцгеймера, вызывали определенное недоумение. Уилкок давно сомневается в исследованиях, в которых утверждается, что используется «очищенный» Aβ*56. Известно, что такие олигомеры нестабильны и спонтанно превращаются в другие типы. Несколько типов амилоида могут присутствовать в образце даже после очистки, поэтому трудно сказать, только ли с Aβ*56 связаны какие-либо когнитивные дефекты, если таковая связь вообще существует. На самом деле, как сообщает Уилкок и другие исследователи, несколько лабораторий безуспешно пытались найти Aβ*56, хотя эти результаты были опубликованы не всеми. Издания часто не заинтересованы в отрицательных результатах исследований, а авторы могут не захотеть создавать противоречия с известными учеными.
Исключение составил Деннис Селкоу из Гарвардского университета, ведущий сторонник амилоидной гипотезы и токсического олигомера, который цитировал упомянутую статью «Nature» не менее 13 раз. В двух статьях 2008 года Селкоу заявил, что не может найти Aβ*56 в жидкостях или тканях человека.
Селкоу по запросу «Science» изучил досье Шрага по документам Лесне и заявил, что находит заключения Шрага достоверными и хорошо доказанными. Селкоу считает, что не каждое изображение является результатом манипуляций, однако, по крайней мере, в случае 12 или 15 изображений нет другого объяснения, кроме как манипуляции. По словам Селкоу, на одном изображении очищенного Aβ*56 в статье «Nature» видны «значимые» признаки подтасовки. То же изображение снова появилось в другой статье, написанной в соавторстве Лесне и Эш, пять лет спустя. Многие другие изображения в работах Лесне могут оказаться неподходящими (или даже ошибочными), а этого более чем достаточно, чтобы бросить вызов ключевой работе, как добавляет Селкоу.
В нескольких спорных статьях Лесне описывается метод, который был разработан для определения олигомеров Aβ отдельно в клетках головного мозга, внеклеточных пространствах и клеточных мембранах. Селкоу вспоминает, как Эш говорила о своем «блестящем докторанте», который его разработал. Он скептически отнесся к заявлению Лесне о том, что олигомеры можно идентифицировать отдельно внутри и снаружи клеток в смеси растворимого материала из замороженной или обработанной ткани мозга. «Все мы, кто слышал об этом, сразу поняли, что это бессмысленно с биохимической точки зрения. Если бы это было реально, все ученые применяли бы такой метод», — отмечает Селкоу. Однако статья в «Nature» зависела от результатов работы, основанной на этом методе.
Сам Селкоу был соавтором статьи 2006 года вместе с Лесне в «Annals of Neurology». Их целью было нейтрализовать действие токсичных олигомеров, но не Aβ*56. В статье присутствует изображение, которое, по мнению Шрага, Бика и Кристофер, было перепечатано как оригинальное в двух последующих статьях Лесне. Селкоу называет факт такого «вопиющим».
Учитывая эти результаты, как продолжает Селкоу, нехватка независимых подтверждений тезисам об Aβ*56 кажется показательной. В науке при публикации трудновоспроизводимых результатов исследования необходимо быть серьезно обеспокоенным тем, что эти результаты могут не соответствовать действительности. Очень мало ясных доказательств того, что Aβ*56 существует, а если и существует, то неизвестно, коррелирует ли его наличие с признаками болезни Альцгеймера в эксперименте (на животных моделях).
Всего Шраг или Бик выявили более 20 подозрительных статей Лесне; 10 были посвящены Aβ*56. В начале текущего года Шраг связался с представителями нескольких изданий, а Лесне с соавт. недавно опубликовали две поправки к своим ранним работам. Одна из них (для статьи 2012 года в «The Journal of Neuroscience») заключалась в замене нескольких изображений (которые Шраг отмечает как проблематичные, указывая, что более ранние версии данных изображений были «обработаны ненадлежащим образом»). Но Шраг считает, что даже на исправленных изображениях видны многочисленные признаки искажения полос, а в одном случае — даже полная замена изображения блота.
Статья в «Brain» от 2013 года, в которой Шраг указал на несколько изображений, также в значительной степени была исправлена авторами в мае 2022 года. Лесне и Эш были первым и старшим авторами исследования, соответственно, в котором демонстрировались «несущественные» значения концентрации Aβ*56 у детей и молодых людей, однако по достижении людьми 40-летнего возраста концентрации такового лишь неуклонно возрастали. В статье значится, что Aβ*56 «может играть ключевую роль на ранних этапах патогенеза болезни Альцгеймера». Авторы заявили, что внесенное ими исправление не повлияло на результаты исследования.
Шраг же не уверен в этом. По его словам, помимо проблем иного рода, на изображении одного исправленного блота присутствуют несколько полос, которые, по-видимому, были добавлены или же удалены искусственно.
Селкоу называет явно сфальсифицированные исправления «шокирующими», особенно в свете гордости Эш статьей «Nature» 2006 года. Он удивлен, как она могла не подвергнуть тщательному анализу все, что так или иначе связано с Aβ*56.
После того, как представители «Science» связались с Эш, она отдельно в PubPeer установила защиту некоторых изображений, в том числе из статьи в «Nature», которые оспаривал Шраг. Она предоставила фрагменты нескольких исходных, неопубликованных версий изображений, на которых не видно очевидных цифровых меток обрезки, обнаруженных Шрагом на опубликованных изображениях. Это говорит о том, что эти метки были безвредными цифровыми артефактами. Тем не менее, на исходных изображениях видно то, что Шраг и Селкоу считают еще более компрометирующим: недвусмысленные доказательства того, что, несмотря на отсутствие явных следов обрезки, изображения нескольких полос блоттинга оказались скопированы и вставлены из соседних областей.
Шраг не мог найти бесхитростного объяснения длинному перечню странностей, тянувшемуся два десятилетия. В одном эксперименте за другим, где применялся вестерн-блоттинг, микроскопия и другие методы возникали серьезные аномалии. Однако он отмечает, что не исследовал исходные изображения с высоким разрешением. Авторы иногда делятся ими с другими исследователями, проводящими аналогичную работу, хотя обычно они игнорируют такие запросы в соответствии с недавней практикой обмена данными. Соглашения об обмене данными не подразумевают наличие доступа для независимых расследователей по делам о противоправном поведении. Лесне и Эш не ответили на запрос «Science» об этих изображениях.
Вопросы о работе Лесне не новы. Клеточный биолог Денис Вивьен, старший научный сотрудник Канского университета, стал соавтором пяти статей Лесне, которые отметили как подозрительные Шраг или Бик. Вивьен защищает обоснованность этих статей, но заявляет, что у него тоже есть причины остерегаться команды Лесне.
Вивьен сообщает, что ближе к концу пребывания Лесне во Франции они вместе работали над статьей о Aβ для «Nature Neuroscience». Во время окончательной проверки он увидел изображения иммунного окрашивания, на которых антитела связываются с белками в образцах тканей, предоставленных Лесне. Эти изображения показались Вивьен сомнительными, и он попросил других студентов повторить эксперимент. Их усилия не увенчались успехом. Вивьен заявляет, что у него возник спор с Лесне, который отрицал противоправные действия. Хотя у Вивьен не было «неопровержимых доказательств» неправомерных действий, он отозвал статью перед публикацией, «чтобы сохранить научную достоверность хотя бы со своей стороны». Потом он разорвал все контакты с Лесне. «Мы никогда не застрахованы от коллег, которые хотели бы обмануть нас, и нам необходимо сохранять бдительность», — заявляет Вивьен.
Шраг выборочно проверил статьи Вивьен или Эш без Лесне. Он не обнаружил никаких аномалий, заключив, что Вивьен и Эш невиновны в фактах данных противоправных действий.
Тем не менее, по словам Уилкок, старшие коллеги-ученые должны уравновесить доверие, что необходимо для укрепления независимости протеже, благоразумной проверкой. Если время от времени необходимо подписывать своим именем изображения, заявлять о себе, публично выступать и получать награды за свою работу, — как в случае с Эш, — необходимо быть уверенным, что все сделано правильно.
Форсайт добавляет: очевидно, что Эш не справилась со своей крайне серьезной обязанностью — задавать сложные вопросы и обеспечивать точность данных. Это было серьезной этической ошибкой.
В своем отчете как анонимного информатора в NIH об исследовании Лесне, Шраг четко обозначил масштабы и ожидания: «Это досье — лишь часть аномалий, легко обнаруживаемых при просмотре общедоступных изображений». Подозрительная работа «не только представляет собой существенную вовлеченность в финансирование со стороны NIH, но и цитировалась… тысячи раз, что, таким образом, может привести к заблуждениям в целой области исследований».
В ответе агентства, которым Шраг поделился с «Science», отмечалось, что жалобы, признанные заслуживающими доверия, будут переданы для рассмотрения в Управление добросовестности исследований (ORI) Министерства здравоохранения и социального обеспечения США. Затем это агентство могло бы поручить университетам-получателям грантов провести расследование до окончательной проверки ORI. Такой процесс может занять годы и оставаться конфиденциальным в отсутствие официального факта неправомерного поведения. Представители издания «Science» заявили NIH, что серьезно относятся к неправомерным действиям в исследованиях, но в остальном отказались от комментариев.
В шумихе вокруг работы Лесне-Эш некоторые специалисты по болезни Альцгеймера видят провал скептицизма, в том числе со стороны изданий, опубликовавших работу. После того, как Шраг связался с «Nature», «Science Signaling» и пятью другими журналами по поводу 13 статей, где одним из авторов был Лесне, некоторые из этих изданий находятся под строгим наблюдением (согласно электронным письмам, которые Шраг получил от редакторов).
По словам Джона Фоули, редактора журнала «Science Signaling», в интервью «Science» существует ряд вполне законных вопросов. Он говорит, что представители его журнала связались с авторами (и сотрудниками университета [UMN]) двух статей за 2016 и 2017 годы, чтобы получить ответ. Он также недавно выразил обеспокоенность по поводу статей.
Представитель журнала «Nature», который публикует стандарты добросовестности предоставления изображений, сообщает, что журнал серьезно относится к опасениям, высказанным по поводу перечисленных статей, но в остальном не дал никаких комментариев. Через несколько дней после запроса от «Science» в «Nature» была опубликована заметка, в которой говорилось, что представители издания ведут расследование по статье Лесне от 2006 года и советуют с осторожностью относиться к ее результатам.
В «The Journal of Neuroscience» присутствует пять подозрительных статей Лесне. Представитель издания заявил, что они следуют рекомендациям Комитета по этике научных публикаций для оценки опасений, но в остальном не дал никаких комментариев.
По словам Форсайта, издания и учреждения, выдающие гранты, не знают, как бороться с подтасовкой изображений. Изображения не подвергаются сложному анализу, хотя инструменты для такого широко доступны. Форсайт заявляет, что это не магия. Важно следить за тем, что отправляется в печать.
Холден Торп, главный редактор «Science», заметил, что редколлегии журналов подвергают изображения все более тщательному изучению, добавив, что 2017 год стал отправной точкой, когда этому начали уделять больше внимания: не только для репутации самого издания, но и для самой науки. Он сослался на структуру отчетности по анализу материального исполнения, разработанную совместно несколькими издателями для повышения прозрачности данных и устранения подтасовок изображений.
Пока федеральные агентства, университеты и издания тихо расследуют находки Шрага, он решил попытаться ускорить процесс, предоставив свои выводы в издание «Science». Он знает, что это может иметь для него личные последствия. Обращаясь к влиятельным агентствам, изданиям и ученым, Шраг мог поставить под угрозу гранты и публикации, необходимые для его собственной карьеры.
Но он говорит, что чувствовал острую необходимость предать огласке работу, которая может ввести в заблуждение специалистов и замедлить поиск лекарства, которое может спасти жизни. Он заявляет, что можно обмануть с целью получения так необходимой публикации; можно обмануть, чтобы получить степень или грант. Но нельзя обманывать, когда идет речь о лечении болезни. «Биологию это не волнует».
Как и усилия по борьбе с Aβ, исследования токсичных олигомеров не привели к появлению эффективных методов лечения. Как заявляет Дэниел Алкон, президент биологической компании «Synaptogenix», который когда-то руководил исследованиями в области неврологии в Национальном институте здравоохранения, многие компании инвестировали миллионы и миллионы долларов или даже миллиарды в разработку растворимых Aβ (олигомеров), и это не привело к какому-то значимому результату.
Шраг считает, что олигомеры могут играть роль в развитии болезни Альцгеймера. Вслед за статьей в «Nature» другие исследователи связывали комбинации олигомеров с когнитивными нарушениями у животных. Все, что связано с олигомерами, потенциально может решить эту проблему. Однако, как продолжает Шраг, это вынуждает нас остановиться и переосмыслить фундамент теорий.
Селкоу добавляет, что амилоидная гипотеза в широком смысле остается жизнеспособной. Он надеется, что люди не падут духом из-за того, что на самом деле выглядит как вопиющий пример неправомерного действия, прямо связанного с олигомерами Aβ. Но если текущие клинические испытания III фазы трех препаратов, нацеленных на амилоидные олигомеры, окажутся неудачными, гипотеза Aβ окажется под большим вопросом.
По словам Селкоу, его беспокоит то, что инцидент с Лесне может еще больше подорвать общественное доверие к науке во времена растущего всеобщего скептицизма. Но ученое сообщество должно показать, что находить и исправлять редкие случаи очевидных проступков вполне реализуемо. Необходимо предать огласке такие факты и предупредить общественность.
«Непосредственный и очевидный ущерб — это финансирование впустую от NIH и пустые умозаключения в этой области, ведь люди используют эти результаты как отправную точку для своих собственных экспериментов» — Томас Зюдхоф
«Нельзя обмануть всех, чтобы вылечить болезнь. Биологию это не волнует» — Мэтью Шраг





