Международная группа биохимиков выяснила, что механизм устойчивости бактерий перед антибиотиками сложнее, чем предполагалось. Чтобы изучить работу гена резистентности, ученые проанализировали структуру рибосомы. Также они разобрались с тем, как некоторым антибиотикам удается воздействовать на устойчивые бактерии.
Некоторые антибиотики при подавлении инфекции атакуют рибосому бактерии. Эта органелла синтезирует белки, а как только ее настигает антибиотик, процесс нарушается и бактерия погибает. Но некоторые штаммы выработали механизм защиты от лекарств — такие бактерии называют антибиотикорезистентными. Проблема устойчивости патогенов перед антибиотиками сейчас стоит крайне остро, ведь чем дольше человечество пользуется старыми лекарствами, тем больше к ним адаптируются бактерии.
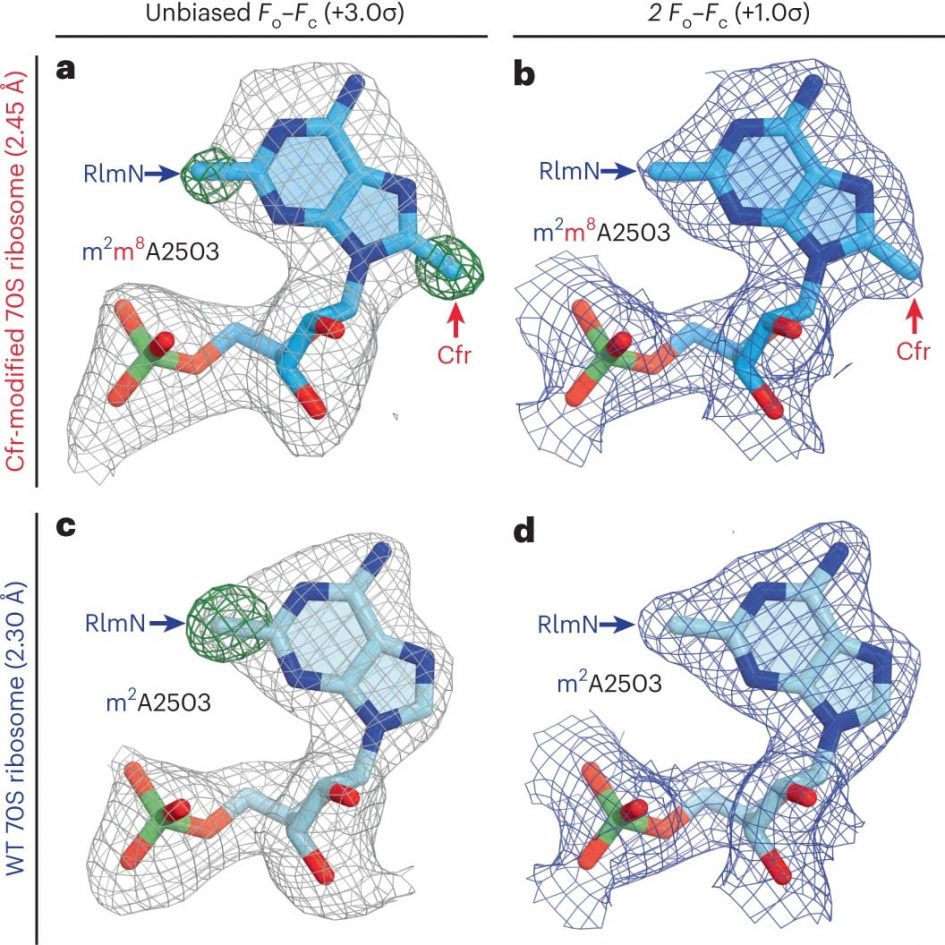
Считалось, что способ защиты заключается в простом блокировании сайта связывания с помощью метильной группы — метилированием. Эту функцию кодирует ген Cfr, который модифицирует рибосому. В результате антибиотику не за что зацепиться и лекарство не срабатывает. Однако исследователи из Университета Иллинойса вместе с коллегами из Гарварда (США) при помощи рентгеноструктурного анализа модифицированной рибосомы узнали, что механизм бактериальной защиты сложнее. Статья об этом опубликована в журнале Nature Chemical Biology.
Чтобы лучше понять механизм блокирования действий антибиотиков, исследователи сконструировали в лаборатории бактериальный штамм с геном Cfr. Они убедились, что этот ген метилирует некоторые нуклеотиды в рибосоме, но не меняет их положения. Но ученые заметили, что под влиянием Cfr нуклеотид A2062 перестает вращаться, как это происходит обычно.
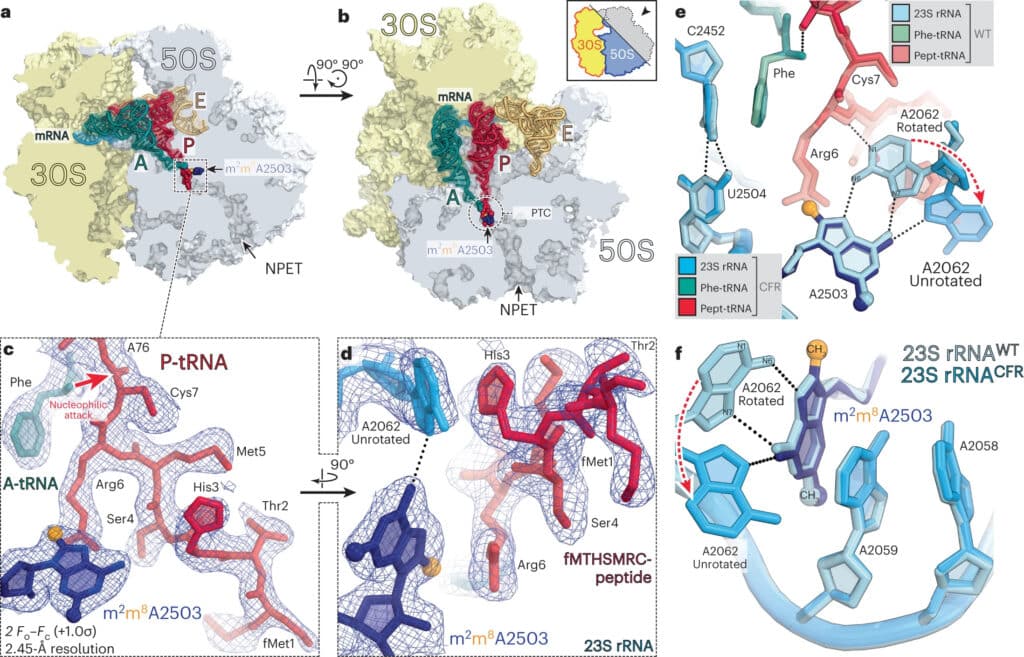
Биохимики предположили, что эта стабилизация нуклеотида может дополнительно снижать эффективность антибиотиков. Чтобы это понять, они нашли в группе устойчивых штаммов те бактерии, где ген Cfr не работает, а вместо него содержатся мутантные версии другого гена. Эта версия тоже останавливает вращение нуклеотида A2062, но метилирования при этом не происходит. Выяснилось, что изменение положения этого нуклеотида в пространстве также препятствует прикреплению лекарственного препарата к рибосоме.
Помимо этого исследователи проверили, как некоторые антибиотики, способны действовать на устойчивые бактерии. Для опытов они выбрали недавно синтезированный ибоксамицин и рассмотрели его структуру во время связывания с модифицированной рибосомой. Биохимики увидели, что форма ибоксамицина позволяет ему проникать в щель сайта связывания.
«Он просто связывается с рибосомами и действует так, как будто ему все равно, было это метилирование или нет. Он легко преодолевает несколько наиболее распространенных типов лекарственной устойчивости», — отметил соавтор работы Юрий Поликанов.
Как считают исследователи, понимание двухкомпонентного механизма защиты резистентных бактерий, а также структура модифицированной рибосомы может помочь в создании антибиотиков нового поколения, активных против штаммов с множественной устойчивостью.