Представители компании Glaxo сообщают, что препарат от изжоги не приводит к развитию опухолей. Но независимые исследователи и собственные ученые предупреждали руководителей компании о данной потенциальной опасности.
Небольшую британскую компанию иногда называли Glaxo University, потому что ею проводились важные фармацевтические исследования, которые редко приводили к созданию прибыльных лекарственных препаратов. Затем ученые из Glaxo Laboratories синтезировали вещество, которое было названо ранитидином, а в 1978 году компания получила патент США. Молекулярный состав препарата был новым, однако не оригинальным. Ученые, как иногда они это делают, вели поиск для создания эффективного лекарства, настолько же эффективного, как и уже существующие, для лечения язвы желудка и для купирования симптома изжоги. Им быстро удалось разработать ранитидин, и Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) США провело ускоренное рассмотрение по его одобрению. Glaxo присвоило ему торговую марку Zantac.
Glaxo рекламировала его как более качественный и безопасный, чем Tagamet (который, собственно, и стал импульсом для создания Zantac), и вскоре Zantac обогнал Tagamet, став самым продаваемым в мире лекарством, отпускаемым по рецепту. В течение многих лет Glaxo почти в половине своих продаж рассчитывала на Zantac и почти на такой же объем прибыли. Компания получила награду от королевы Елизаветы: генеральный директор был посвящен в рыцари. Zantac завоевал себе репутацию и приносил прибыль компании. Благодаря нему родилась современная «версия» Glaxo: после многих слияний, поглощений и иных пертурбаций появилась GSK Plc — компания, которая сегодня стоит около 73 миллиардов долларов. Среди его самых популярных препаратов — антидепрессанты «Паксил» и «Веллбутрин» и вакцина от опоясывающего герпеса «Shingrix».
Однако Zantac ждала иная судьба. В 2019 году было обнаружено, что в составе препарата в высокой концентрации содержится вероятный канцероген. Это было не случайностью или ошибкой нескольких партий. Ранитидин сам является источником опасного вещества. Производители Zantac и регуляторы здравоохранения по всему миру отозвали препарат, а весной 2020 года FDA распорядилось вообще убрать его с рынка. Был наложен запрет на производство этого препарата любыми компаниями; врачи больше не имели права его прописывать. Канцероген, название которого NDMA, когда-то добавляли в ракетное топливо и теперь используют только для того, чтобы вызывать рак в экспериментальных условиях у лабораторных крыс. По заявлениям FDA, потребление незначительных количеств вещества безвредно. Однако благодаря тестам удалось выявить избыточное содержание NDMA в ранитидине, а само вещество, оказалось, может синтезироваться в еще больших объемах с течением времени. Ни один из вариантов применения препарата не рассматривался как безопасный.
Более 70 000 человек, принимавших Zantac и его дженерики, подали иски компании Glaxo.
С самого начала и до конца выпуска ранитидина представителей компании Glaxo предупреждали о потенциальной опасности их собственные ученые и независимые исследователи. Отчеты за прошедшие четыре десятилетия содержатся в сотнях документов, на тысячах страниц, многие из которых никогда не публиковались. Команда Bloomberg Businessweek проанализировала судебные документы, многие из которых все еще засекречены, а также исследования, стенограммы FDA и новые заявки на одобрение лекарств, полученные по запросам, согласно Закону о свободе распространения информации. В них говорится, что представителями FDA при одобрении ранитидина риск развития рака в расчет принимался. Однако компания Glaxo не «поделилась» критически важным исследованием. На протяжении многих лет компания также поддерживала проведение некорректных исследований, направленных на минимизацию проблем с препаратом, а также было отдано предпочтение транспортировать и хранить лекарства таким образом, что могло бы не вскрыть проблему. Компания Glaxo продавала препарат, который потенциально нес угрозу людям, пыталась сбрасывать со счетов доказательства этого и никогда не предупреждала об этом.
Более 70 000 человек, принимавших Zantac или его дженерики, предъявили иски компании в судах штатов США за продажу потенциально ядовитого и опасного препарата. Предполагается, что первый судебный процесс начнется в конце февраля 2023 г. в Верховном суде Калифорнии в округе Аламеда, однако, по всей видимости, он будет отложен до лета (в связи с рабочим графиком самого судьи). Другие компании, которые продавали Zantac в последующие годы, в том числе Pfizer Inc. и Sanofi, также оказались объектами судебных исков.
В декабре GSK добилась положительного решения по определенной группе дел в федеральном суде. Окружной судья США Робин Розенберг в Южном округе Флориды отклонила тысячи федеральных исков, которые были собраны в ходе ее процесса для досудебного разбирательства. Она заявила, что в научном сообществе не получила широкого признания наблюдаемая, статистически значимая связь между приемом ранитидина и развитием рака. GSK рассматривает последнее слово Розенберг как «вердикт» относительно всех этих претензий. Представитель компании Кэтлин Куинн заявила, что мнение суда согласуется с позицией, которую GSK и другие соответчики занимали на протяжении всего судебного процесса. Спустя более чем три года обширных испытаний, включая 13 рецензируемых эпидемиологических исследований, проведенных с целью изучения данных об использовании ранитидина у людей, был сделан научный вывод об отсутствии последовательных или надежных доказательств, что Zantac (ранитидин) повышает риск развития любого типа рака. Адвокаты, представляющие тех, кто подал иски, планируют подать апелляцию.
GSK все еще приходится вести тяжбы с десятками тысяч дел, ожидающих рассмотрения в судах штатов, где судьи не связаны решением федерального суда. Согласно заявлению представителей компании, активная защита ее будет продолжена, в том числе от всех претензий в ходе этого судебного процесса. В GSK от дальнейших комментариев воздержались.
Представители каждого агентства общественного здравоохранения — от Агентства по охране окружающей среды до FDA и Всемирной организации здравоохранения — говорят, что NDMA, по всей видимости, вызывает рак у людей. Однако доказать, что раковые клетки конкретного человека подверглись мутации вследствие воздействия препарата компании GSK, сложно. Решения Glaxo свидетельствуют о том, что такая вероятность никогда даже не рассматривалась. Однако зацепки всё таки были. Согласно документам, представители Glaxo предпочитали не обращать на них внимания.
NDMA — это аббревиатура N-нитрозодиметиламина; вещество представляет собой желтую жидкость, растворяющуюся в воде, без запаха и особого вкуса. Впервые связь этого соединения с раком была обнаружена в 1956 году; вещество оказалось наиболее токсичным для печени. Оно относится к группе химических соединений, называемых нитрозаминами, которые на момент 1970-х гг. считались самыми сильными канцерогенами из когда-либо обнаруженных. В экспериментах, оно вызывало рак у всех видов испытуемых животных.
Однократная доза менее 1 миллиграмма NDMA может привести к мутации клеток у мышей и стимулировать развитие опухолей, а 2 грамма способны привести к летальному исходу у человека в течение нескольких дней.
В 1969 году Уильям Лижински работал исследователем в области онкологии на правительство США. Он определил, что нитрозамины могут образовываться в желудке. Нитриты — распространенные химические вещества, содержащиеся в вяленом и жареном мясе, а также в пиве, кофе и овощах. В этих продуктах они могут содержатся вместе с другой группой химических веществ — аминами — соединениями, являющимися компонентами многих лекарств. Кислота в желудке создает идеальные условия для протекания реакции. Количество нитрозаминов, синтезируемых за один раз незначительно, однако с течением времени может стать угрожающим.
Лижински опубликовал исследования о нитрозаминах. Он свидетельствовал перед Конгрессом, считая, что самый простой способ минимизировать угрозу — ограничить количество нитрита натрия, которое производители пищевых продуктов могут добавлять в качестве консерванта и для ароматизации мяса. Ветчина, бекон, пастрами, солонина, колбаса — употребление этих продуктов, как оказалось, часто вызывает изжогу и кислотный рефлюкс.
Также он изучил различные амины (всего несколько сотен), чтобы увидеть, какие из них могут образовывать нитрозамины в моделируемых условиях желудка. Результаты изучения показали, что все. Ранитидина еще не существовало, однако у него тоже аминовая структура. Исследования Лижински, проведенные в 1979 году, привели к тому, что антигистаминный препарат, обычно используемый в качестве седативного средства, был изъят из продажи из-за канцерогенных особенностей.
Розали Лижински, генетик-токсиколог, недавно уволившаяся из FDA, изучала нитрозамины вместе со своим мужем. Она рассказывает, что Уильям думал, что амины были самыми важными канцерогенами. Однако его исследования лишили федерального финансирования — в основном, по ее словам, из-за давления со стороны пищевой и фармацевтической промышленности. Уильям умер в 2004 году после инсульта, считая свою работу бесполезной.
В ноябре 1980 года видный фармацевтический аналитик известной британской инвестиционной компании разослал инвесторам отчет под названием «Glaxo, ранитидин — повод для беспокойства». Glaxo готовилась получить разрешение FDA на продажу ранитидина в США. Аналитик писал, что согласно результатам фундаментальных исследований в США, при определенных условиях в желудке ранитидин может образовывать потенциально опасное соединение. Такими условиями и была химическая реакция, которую описывали Лижински и другие; продукт этой реакции и может вызвать рак. Для компании это стало причиной беспокойства: вырисовывалось возможное влияние на продажи. Аналитик предупреждал, что до тех пор, пока споры о связи ранитидина с раком не будут решены, врачи общей практики в США могут отказываться в назначении препарата.
После выхода отчета этого аналитика, глава отдела по связям с общественностью Glaxo Джефф Поттер предостерег общественность от чрезмерной реакции. Он написал служебную записку Полу Джиролами, генеральному директору, который еще не был сэром Полом [еще не был посвящен в рыцари королевой Елизаветой — прим. перев.], председателю правления компании Остину Байду, который уже был сэром, и другим членам правления. В ней Поттер пообещал: «Мы будем крайне внимательно следить за ситуацией, чтобы предлагать быстрые действия для защиты компании, если положение ухудшится». Позже в показаниях, исполнительный директор, который тогда был заместителем директора Glaxo по клиническим исследованиям, сказал, что правление компании никогда не просило провести испытания для проверки ранитидина на предмет образования соединений нитрозаминов из данного препарата.
В одном испытании, проведенном в Великобритании летом 1981 года, 11 здоровых мужчин получали по 150 мг ранитидина два раза в день: утром и вечером, в течение четырех недель. Ученые Glaxo пытались выяснить, может ли длительное употребление ранитидина воздействовать на бактерий желудка, особенно на производящие нитриты, что способствовало бы образованию нитрозаминов. Было обнаружено, что это возможно, однако затем следовал вывод, что клиническая значимость этого неясна. Позже в FDA рассмотрели резюме, где ученые Glaxo писали, что высокие уровни нитритов могут образовывать нитрозамины, почти все из которых являются канцерогенами. В то же время исследования на животных, проведенные до сих пор, не продемонстрировали канцерогенность ранитидина, поэтому степень его риска для человека не может быть оценена. Кроме того, пациенты не должны были принимать препарат долго. «Ранитидин рекомендуется только для кратковременного применения, — заключили ученые, — и поэтому канцерогенный риск, если таковой имеется, сведен к минимуму».
Но в конечном счете, многие люди принимали Zantac месяцами, а порой годами и даже десятилетиями.
В октябре 1981 года Glaxo объявила о планах построить завод в Северной Каролине, на котором производился бы Zantac. Препарат уже продавался в Великобритании и Италии, а исследователи изучали его. Сильвио Де Флора из Университета Генуи опубликовал свои результаты в британском медицинском журнале Lancet, в котором показал, что при смешивании ранитидина с нитритом возникают «токсические и мутагенные эффекты». Де Флора не пытался выяснить причину токсичности; позже, он предложил всем, кому прописан Zantac, ограничить потребление нитритов и принимать препарат задолго до или после еды. Во всем мире, согласно инструкции, для предотвращения изжоги Zantac рекомендуется принимать перед едой.
Руководители Glaxo немедленно связались с Де Флора. «Они пытались убедить нас [исследователей из Университета Генуи] в безопасности ранитидина», — рассказал он журналистам из Bloomsberg в своем ответе по e-mail. «Фармацевтические компании не любят исследования такого рода», — добавляет Де флора.
Двумя неделями позже пятеро ученых из Glaxo опубликовали письмо в журнале Lancet, чтобы, по их словам, представить выводы Де Флоры в перспективе. Они отметили, что Де Флора использовал такие концентрации нитритов, достичь которых в желудке человека никогда не было бы возможно. Это стало стандартным аргументом представителей Glaxo. Де Флора сообщает, что исследователи обычно используют высокие дозы тестовых соединений в лабораторных экспериментах потому, что производится оценка конкретного эффекта за короткое время, по сравнению с более распространенной ситуацией воздействия низких доз в течение длительных периодов времени.
В марте 1982 года в Glaxo узнали о другом исследовании, в котором раскрывалась потенциальная опасность ранитидина. Отчет объемом всего несколько страниц был отправлен компании ее конкурентом Smith, Kline & French, производителем Tagamet. Исследователи также комбинировали ранитидин с различными концентрациями нитрита и также наблюдали образование ядовитых веществ. Они назвали его в честь Glaxo: NDMA.
Скептицизм в Glaxo был естественной реакцией: ученые из компании-конкурента протестировали продукт [т.е., ранитидин] и обнаружили недостаток. Руководство Glaxo потребовало провести собственные тесты: эта задача была возложена на Ричарда Таннера, который работал в отделе биохимической фармакологии. Он получил такие же результаты. В некоторых образцах он определил до 232 000 нанограммов NDMA. Позже FDA сочло, что небольшое количество NDMA приемлемо в любом лекарстве, за минимальное референтное значение было взято 96 нг. Когда Таннер использовал более низкий уровень нитритов, который теперь, по словам компании, ближе к реальным условиям в желудке человека, NDMA обнаружено не было. Но еще в 1982 году, как показывают судебные документы, Glaxo держала исследование в секрете. Заместителю директора по клиническим исследованиям в США никогда не говорили об отчете Таннера. Главный медицинский советник по исследованиям желудочно-кишечного тракта не был осведомлен об этом. Так было и с FDA.

Отчет Таннера, который компания Glaxo держала в тайне почти сорок лет
В Glaxo также знали и о другой потенциально серьезной проблеме с ранитидином: препарат не был стабилен. Он был чувствителен к воздействию тепла и влажности, и при воздействии слишком большого количества любого из этих параметров мог распадаться. Позже на этом сосредоточится FDA: в определенных условиях ранитидин начинает разлагаться. Условия должны быть не обязательно экстремальными, иногда даже при нормальной комнатной температуре. Это создает условия для образования NDMA уже в самом препарате.
В 1982 году компания пыталась предотвратить разложение инъекционной формы ранитидина. Glaxo только что подала заявку на продажу таблеток ранитидина и вскоре собиралась добиваться одобрения для инъекционной формы препарата. Джон Падфилд, глава отдела фармацевтических разработок, настаивал на том, чтобы эта форма ранитидина хранилась в охлажденном состоянии при температуре 4°C (39°F), поскольку она была доставлена из Великобритании, транспортирована по США и хранилась на региональных складах. В марте он писал, что не соблюдать данную холодовую цепочку было бы «крайне опасно». Несколько месяцев спустя в июльском меморандуме руководители компании написали: «Охлаждение инъекционной формы ранитидина неприемлемо для маркетинга Glaxo». Падфилд был непреклонен. «Продукт очень чувствителен к температуре, — писал он в ответ. — Крайне важно, чтобы защита продукта была осуществлена тем надлежащим образом, как это обсуждалось».
В Северной Каролине дела пошли быстро. Первые испытания ранитидина на людях в США начались всего за два года до того, как Glaxo подала заявку на новый препарат в марте 1982 года. Однако Фред Эшельман, который тогда занимал должность Заместителя директора по клиническим испытаниям, сообщил, что предприятие было небольшим, а штат состоял преимущественно из молодых людей, и безопасность никогда не ставилась под угрозу, а им не приходилось иметь дело с большим количеством бюрократии. Он продолжает, что все полагали тогда, что это отличное лекарство: «Чем быстрее мы сможем вывести его на рынок, тем быстрее пациенты смогут его использовать. Мы все были преданы хорошим идеалам». Эшелман был среди многих, кому следовало увидеть исследование Таннера, однако этого не произошло. Сейчас он отказывается это комментировать, но сообщил следующее: «Если бы этот препарат был токсичен сам по себе, нам бы давно это стало известно ».
В мае 1982 года Эшельман и группа ученых Glaxo собрались в Национальной медицинской библиотеке, чтобы представить дело о Zantac группе независимых исследователей и группе должностных лиц FDA. Группа собиралась рекомендовать препарат к одобрению FDA для продажи в США.
Дэвид Джек, который помог синтезировать ранитидин, начал собрание своей речью первым. Он отметил, что компания провела обширные токсикологические исследования ранитидина и не обнаружила ничего подозрительного. Он считал, что в то утро было необходимо сосредоточиться только на том, что вызывает у людей настоящую проблему — на вероятности канцерогенеза вследствие приема подобных препаратов. Наряду с другими учеными Glaxo он представил три исследования, согласно которым следовало, что длительное использование ранитидина (более двух лет) не приводит к развитию рака у крыс или мышей. Ранитидин оказался исключительно нетоксичным соединением, заявил один из коллег Джека. «Доказательства того, что ранитидин сам по себе является канцерогеном ни в желудке, ни где-либо еще, отсутствуют».
Ученые Glaxo оспаривали идею того, что ранитидин может образовывать нитрозамины в любых нормальных условиях человеческого организма. Ими не было упомянуто исследование, проведенное Таннером. Ричард Кляйн, проработавший в FDA более 40 лет, в том числе с командами по одобрению лекарственных препаратов (хотя и не с Zantac), говорит, что если бы представители агентства знали об исследовании Таннера, это могло бы, по крайней мере, «вдохновить FDA задать больше вопросов, запросить дополнительные данные. Это могло бы вызвать подозрения FDA».
Как бы то ни было, обсуждение перешло от любых опасений относительно развития рака к конкретным дозировкам и типам язв [желудка и двенадцатиперстной кишки], которые Zantac способен вылечить. Разговоров о том, как нужно транспортировать и хранить препарат, а также какие предупреждения, если таковые имеются, должны быть указаны на этикетке, не было. Темп был быстрым. Прямо перед обеденным перерывом сторонние специалисты проголосовали за то, чтобы рекомендовать FDA одобрить препарат. Они предлагали применять его по 150 мг два раза в сутки в течение восьми недель для лечения острой язвы двенадцатиперстной кишки, наиболее распространенного вида данной патологии. В конечном счете, в инструкцию к препарату обязательно включались указания по хранению таблеток в домашних условиях в сухом месте, при температуре не выше 86F [30 градусов С]. Год спустя, в мае 1983 года, FDA выдало разрешение Glaxo на продажу Zantac. The New York Times писала, что препарат, который уже продавался в 31 стране, был в несколько раз более мощным, чем Tagamet, а также обладал меньшим количеством побочных эффектов. Оба препарата считались настолько безопасными, что врачи прописывали их для гораздо более широкого круга жалоб пациентов, связанных с заболеваниями желудка, чем предлагали в компании.

Одобрение Zantac в США, фото оригинального документа, 1983 г.
Продажи Zantac в США в первый год составили около 125 миллионов долларов, что сделало его одним из лучшим вводом препарата на фармацевтический рынок за всю историю. Как сообщает Джо Грейдон, фармаколог из Северной Каролины (один из основателей People’s Pharmacy — организации по охране здоровья потребителей), благодаря Zantac, Фред Эшельман стал героем Glaxo. Глава компании Glaxo сравнил Zantac с локомотивом, который тянет весь поезд. Грейдон продолжает, что препарат был и источником дохода, и огромным убийцей. Эшельман основал собственную фирму, которая проводила испытания новых лекарств для фармацевтических компаний. Впоследствии к нему присоединятся несколько руководителей из Glaxo. В 2011 году он продал бизнес за 3,9 миллиарда долларов, а позже пожертвовал 100 миллионов долларов фармацевтической школе Университета Северной Каролины в Чапел-Хилл. Учебное заведение было названо в его честь.
Маркетинговая кампания Glaxo стала мастерской попыткой подорвать Tagamet, на тот момент самый продаваемый рецептурный препарат в мире. Управленцы компании знали, что в одной таблетке Zantac содержится больше активного ингредиента, чем в Tagamet, поэтому рекламировали его как более эффективный. Они знали, что Zantac будет назначаться пациентам два раза в сутки, вместо четырех и акцентировали внимание клиницистов, что он удобнее. Они понимали и то, что некоторые пациенты страдали от побочных эффектов Tagamet — плохого взаимодействия с другими лекарствами и спутанности сознания. Zantac продавался как более безопасный препарат. А цену на Zantac компания Glaxo ставила примерно на 15-25 % выше, как доказательство большей эффективности по сравнению с Tagamet. Smith, Kline & French развернули собственную рекламную кампанию в поддержку Tagamet, позиционируя препарат как «экспертное средство при язве».
Glaxo увеличила свой торговый персонал втрое, вступив в сотрудничество со швейцарской фармацевтической компанией Hoffmann-La Roche, у которой в то время был большой штат сотрудников, однако в «арсенале» не было по-настоящему крупных препаратов. Как и ожидалось, они начали маркетинговую кампанию Zantac для гастроэнтерологов, а затем, что было менее ожидаемо, начали проводить «образовательные симпозиумы» для врачей первичной медико-санитарной помощи, остеопатов и фармацевтов.
Через три года после того, как Zantac был представлен в США, FDA вынесло Glaxo выговор за неоднократные ложные рекламные заявления. Например, такое произошло, когда компания стремилась получить право на участие в государственных льготных программах. В мае 1986 года в четырехстраничном письме FDA содержались следующие слова: «По-видимому, нам не удалось добиться добровольного исправления этой рекламно-пропагандистской деятельности со стороны вашей компании». Письмо заканчивалось угрозой принятия мер со стороны контролирующих органов. Представители Glaxo ответили, что агентство неверно истолковало действия компании.
В том же году Tagamet стал первым лекарством, объем продаж которого достиг миллиарда долларов. В следующем году Zantac обогнал его.
В марте 1988 года Glaxo заказала опрос Гэллапа с заголовком «Изжога по всей Америке». Было установлено, что 44 % взрослого населения ежемесячно испытывали симптомы изжоги. К тому времени врачи уже могли прописывать Zantac от изжоги, но было доступно множество антацидов, которые продавались без рецепта. Glaxo запустила рекламную кампанию этого опроса по телевидению и в прессе. В рекламе отмечалось, что изжога и другие симптомы хронического рефлюкса могут свидетельствовать о язве, после чего предлагалось обратиться к врачу.
Один уважаемый гастроэнтеролог из Северной Каролины зимой 1988 года провел исследование, которое показало, что Zantac способствует уменьшению выраженности изжоги у бегунов: новой группы потенциальных пациентов с патологией, получившей свое наименование недавно [на тот момент], — рефлюксом бегунов. Исследование было небольшим и никогда не рецензировалось, однако известность доктора и агентство по связям с общественностью компании Glaxo приковали внимание к нему. Позже, The New York Times сообщила, что доктор был платным консультантом Glaxo. Исследователь же заявлял, что не думал, что компания извлечет выгоду из исследования.
К 1989 году объем продаж Zantac составил 2 миллиарда долларов. На его долю приходилось половина продаж Glaxo и 53 % всего рынка рецептурных средств от язвы.
В 1993 году FDA перешла к исполнению собственных угроз относительно маркетинга Zantac. В своем предупредительном письме агентство заявило, что Glaxo «многократно предприняла действия рекламного характера» для распространения вводящей в заблуждение информации о том, что Zantac превосходит по эффективности Tagamet. Агентство потребовало объяснений в письменном виде от Glaxo перед американскими врачами, а также опубликовала рекламу в 12 ведущих медицинских журналах, для исправления любых подобных заявлений. Представитель FDA в интервью лондонской газете Sunday Times заявил, что большинство компаний не допускают ошибок в рекламных материалах, а Glaxo пошла по наихудшему сценарию Через два месяца компания запустила свою «исправленную» рекламную кампанию.
У Glaxo было много причин для сотрудничества с FDA. Среди прочего: компания работала над разработкой низкодозных безрецептурных версий Zantac для лечения изжоги. Ожидалось одобрение FDA. Еще одним изменением, которое рассматривали управленцы компании, был цвет таблеток. При проведении тестов на стабильность таблетки белого цвета становились желтыми и коричневыми, что Glaxo попыталась скрыть. Разработчики остановили свой выбор на розовом покрытии из оксида железа для новых таблеток. Чаще всего изменение цвета — это признак разложения таблетки. В некоторых случаях деградация может привести к образованию опасных примесей. В Glaxo заявили, что это не имеет отношения к Zantac. Йэн Уинтерборн, который работал над разработкой безрецептурной версии препарата, заявил, что в оболочке был использован цвет, способный обеспечить однородный внешний вид таблеток на протяжении всего срока их хранения. «Процессы распада вещества, признаком чего было изменение цвета препарата, больше не были проблемой”, — заключил он.
Когда Glaxo подала заявку на безрецептурную форму Zantac, Уинтерборн стал одним из многих получателей поздравительного электронного письма. В письме, которое писал один из руководителей в 1994 г., значилось: «На этом завершается то, что я считаю героическим усилием всех участников этого проекта за последние два с половиной года. Это одно из самых значительных достижений Glaxo за все время».
Весной 1996 года Glaxo выпустила безрецептурную форму Zantac 75 мг. Таблетки были розового цвета, их можно было принимать один или два раза в день. Суммарно американцы тратили около миллиарда долларов ежегодно на облегчение симптомов изжоги. Маркетологи Glaxo запустили рекламную кампанию, а слоганом стала фраза: «Легенда жива».
В 1995 году Glaxo завершила враждебное поглощение другой британской фармацевтической компании Wellcome. Пять лет спустя, в 2000 году, Glaxo Wellcome приобрела своего давнего конкурента, известного тогда под наименованием SmithKline Beecham. Это было крупнейшее слияние в истории отрасли, в результате которого была создана крупнейшая в мире фармацевтическая компания GlaxoSmithKline.
В то же время Джеймс Гетц, авиационный инженер из Южной Калифорнии, уже много лет принимал Zantac: сначала по рецепту, затем безрецептурную форму. После того, как FDA одобрило дженерики, он принимал и их. У Джона Рассела, живущего недалеко от Лос-Анджелеса, был диагностирован гастрит, и в 2001 году он начал принимать препараты, приобретая их на местных заправочных станциях и в аптеках.
Проблема с обесцвечиванием Zantac сохранялась. В 2010 году Эндрю Сирла, курировавшего оценку риска генотоксичности в GSK, попросили выяснить, почему инъекционные формы Zantac желтеют. В ходе исследования Сирл проверил примеси, которые вызывали такое желтое обесцвечивание. NDMA, применяемые в лабораториях, желтого цвета, однако это соединение не подверглось проверке. Проблема снова возникла в 2015 году, когда с производственной площадки в Китае пришли сведения о проблемах с обесцвеченными и испорченными таблетками Zantac. GSK рассылала клиницистам письма, в которых говорилось, что компания не смогла идентифицировать какие-либо конкретные примеси [ответственные за изменение цвета]. Однако подтверждений тому, что таблетки, ставшие коричневыми, соответствуют ее стандартам безопасности, не было. Тем не менее никто не искал NDMA. В своих показаниях Сирл указывал ненадлежащее хранение препарата.
Между этими двумя инцидентами было еще два, не связанных с Zantac, которые вызвали нежелательную проверку GSK контролирующими структурами. В 2012 году компания согласилась признать себя виновной и выплатить штраф в размере 3 миллиардов долларов за продажу лекарств ненадлежащих характеристик, игнорирование данных о безопасности и обман системы Медикейд. После Zantac самыми продаваемыми препаратами у компании были Paxil, Wellbutrin и средство от сахарного диабета Avandia. Министерство юстиции США назвало это крупнейшим урегулированием мошенничества в сфере здравоохранения в истории США и крупнейшим платежом, когда-либо произведенным фармацевтической компанией. Два года спустя Китай оштрафовал GSK на 500 миллионов долларов и депортировал топ-менеджера за подкуп врачей для выписывания рецептов. Представители компании сообщили ВВС, что «опубликовали заявление с извинениями перед китайским правительством и его народом».
В 2017 году, в возрасте 60 лет, Гетцу диагностировали рак мочевого пузыря. Это само по себе не было чем-то необычным; в возрасте 60 лет этот тип рака часто диагностируется у мужчин. Часто, раком мочевого пузыря заболевают курильщики, но Гетц не курил с 22 лет. Его работа не была связана с воздействием каких-либо потенциально вредных химических веществ. Это было странно, но он не воспринял диагностированный рак как что-то неслучайное. Несчастный, страшный диагноз, однако случайный. Онколог удалил опухоль и прописал курс иммунотерапии. Затем Гетц и врачи предприняли тактику выжидания. Очень часто наступает рецидив рака, который оказывается крайне агрессивным. Врачу пришлось удалить Гетцу мочевой пузырь и простату, а также 20 футов его кишечника. После этого у пациента развилась мочекаменная болезнь и сепсис. Гетц будет первым из тысяч, кто подал иск в суд против GSK. По этой причине его адвокаты советовали ему отказаться от комментариев этой истории.
В сентябре 2019 года FDA получило 19-страничный документ, в котором были сделаны некоторые тревожные заявления касательно ранитидина. Представители Valisure, частной лаборатории, работающей независимо от FDA, заявили, что обнаружили чрезвычайно высокие концентрации NDMA в Zantac и нескольких непатентованных формах ранитидина. Лаборатория Valisure начала проведение тестов по выявлению NDMA за год до того, как FDA отозвало несколько партий валсартана (препарата для лечения артериальной гипертензии), поскольку они были контаминированы этим соединением. Но с ранитидином ситуация казалась хуже. Valisure обнаружила NDMA в каждой исследованной форме ранитидина и заключила, что проблема связана с самим действующим веществом.
FDA выпустило предупреждение, но также поставило под сомнение используемый Valisure метод тестирования. В агентстве заявили, что проведут собственные тесты по своим протоколам. В течение месяца по меньшей мере в двух десятках стран ранитидин был изъят из продажи или же его распространение было прекращено. GSK, которая к тому времени продала права на продажу Zantac в США, действовала самостоятельно, чтобы остановить поставки препарата. То же самое сделали Sanofi, французская компания, которая приобрела права в США в 2017 году у Boehringer Ingelheim GmbH, и Pfizer, которая продавала Zantac с 1998 по 2006 год.
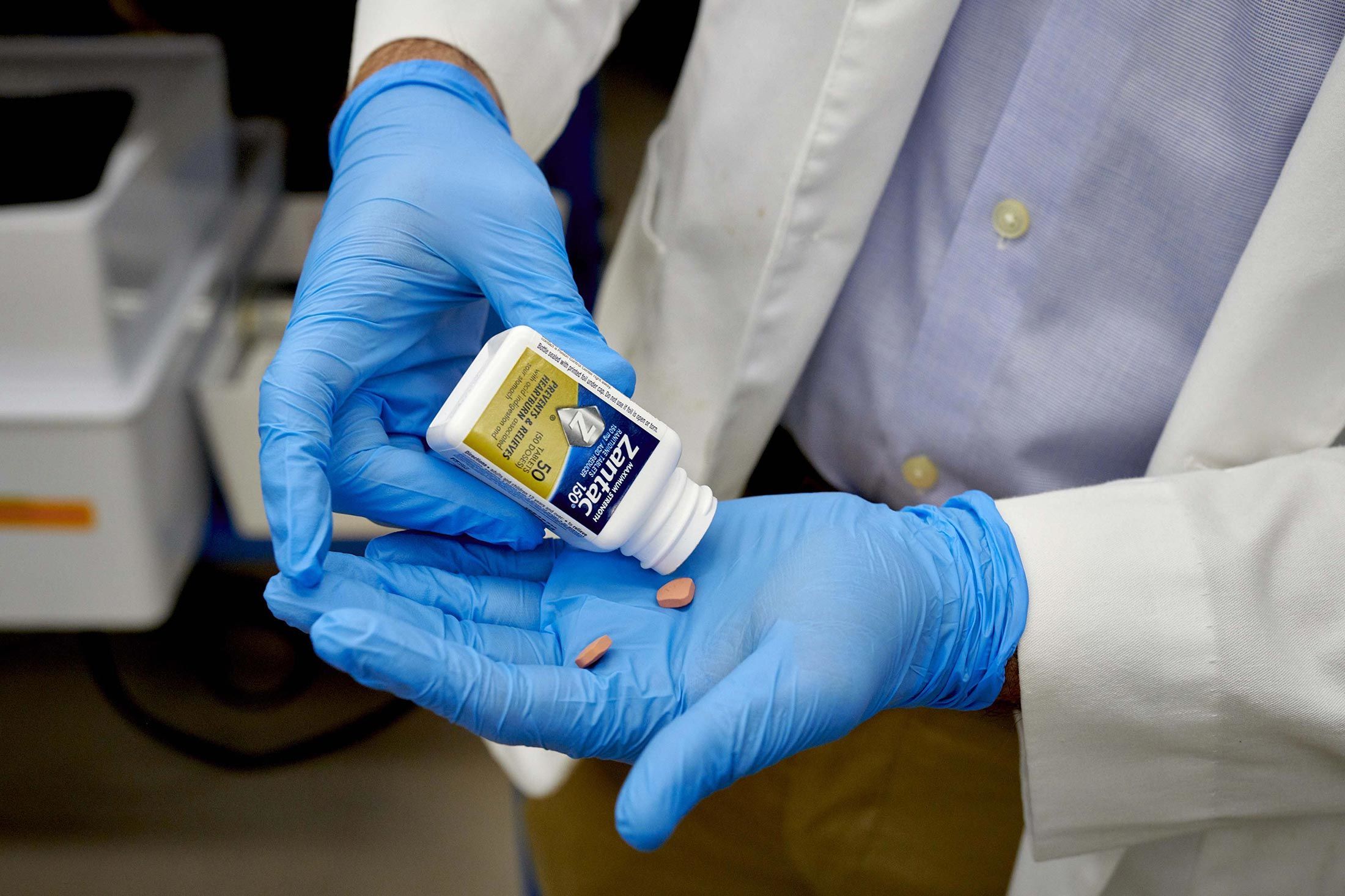

Ученые проводят тесты препарата Zantac в лаборатории Valisure, которая предупредила FDA об опасности в 2019 г.
В апреле 2020 года FDA приняло редкое и радикальное решение: агентство обязало производителей ранитидина — любой версии и дозы — полностью прекратить производство и продажу препарата. В сообщении агентства значилось, что уровни NDMA повышаются в ранитидине даже при нормальных условиях хранения. Было обнаружено, что его концентрация значительно увеличивается в образцах, хранящихся при более высоких температурах, например, при которых препарат распространяется по торговым точкам и при обороте с потребителями. Грейдон из People’s Pharmacy называет это «первым примером, когда условия хранения могут серьезно влиять на качество лекарств, и FDA признает это».
Только в октябре 2021 года FDA поделилось некоторыми подробностями того, что обнаружили сотрудники агентства, и это было сделано не в опубликованной статье, а во время ежемесячной серии лекций под названием FDA Grand Rounds. Представители агентства заявили, что при первоначальном тестировании одна таблетка ранитидина в прохладной мятной форме содержала 357 нг NDMА. Это почти в четыре раза больше порога FDA для любого препарата. А пять месяцев спустя содержание этого соединения достигло уже 931 нг.
В FDA отказались комментировать какое-либо взаимодействие с Glaxo, но в своем заявлении представители агентства указали, что ведется работа над обеспечением доступа к безопасным, эффективным и качественным лекарствам, проводится оценка преимуществ и рисков «в соответствии с современной наукой»; требуется убрать препарат с рынка, где это возможно; «когда выявляются новые примеси, используются новые производственные процессы или когда научный прогресс делает шаг вперед, FDA работает над повышением безопасности, качества и эффективности и будет продолжать исследования рисков для здоровья пациентов». Решение агентства вывести ранитидин с рынка было основано на том, что NDMA образуется в самом препарате, а не в желудке. FDA сообщает, что после приема внутрь ранитидин не вызывает образования большего количества NDMA. Некоторые ученые не согласны с данным утверждением.
В декабре 2020 года GSK опубликовала результаты так называемого анализа первопричин. Это было неубедительно: ученые компании не могли точно определить, как NDMA образуется в ранитидине и отметили, что еще в 1970-х годах, когда препарат был впервые разработан, никто не мог точно предсказать, возможно ли образование NDMA.
Шесть месяцев спустя FDA приняло еще одно редкое и последовательное решение. Несмотря на то, что в самом ранитидине был обнаружен NDMA, и хотя препарат является вероятным канцерогеном для человека, представители агентства заявили, что явные признаки того, что Zantac повышает риск развития рака, отсутствуют. Это значится на восьмой странице 10-страничного исследования, посвященного изучению концентраций NDMA в моче людей, принимавших ранитидин. Заявление основывалось на семи статьях сторонних ученых. Один из них показал связь между ранитидином и раком молочной железы, однако подвергся критике со стороны агентства за примененные методы. Также были опасения по поводу рака печени, но авторы заявили, что у них еще недостаточно данных для подтверждения связи. Вывод FDA не казался окончательным, но для Glaxo оказался неотъемлемой частью пиара и, предположительно, юридической защиты. Некоторые ученые называют это «невиновностью по ассоциации». С тех пор, в трех исследованиях была выявлена связь между препаратом и раком, особенно новообразованиями мочевого пузыря и печени. Представители FDA сообщили, что поддерживают свое раннее заявление, которое, по утверждениям критиков, также освобождает агентство от ответственности за то, что нахождение опасного химического вещества в лекарстве скрывалось десятилетиями.
Через некоторое время эффективность безрецептурных таблеток Zantac, которые принимал Джон Рассел, оказалась недостаточной для купирования симптомов изжоги, и в 2017 году врач прописал ему суточную дозу 300 мг. Полтора года спустя Рассел заметил кровь в моче. Онкологи обнаружили у него в мочевом пузыре 3-сантиметровую опухоль. Расселу, как и Гетцу, сказали, что после радикального лечения рак, вероятно, может рецидивировать. Так и произошло. По словам Рассела, его лечащий врач был сбит с толку. Он никогда не курил (курение — это самый значимый фактор риска), не работал с химикатами или пластиком, у него отсутствует отягощенная по раку наследственность. Также Рассел добавляет, что прежде никогда не слышал о риске развития рака мочевого пузыря. Опухоль выявлялась в ходе каждой цистоскопии, которую мужчина проходил с 2021 года; он перенес четыре операции за последние 18 месяцев.
Узнав об отзыве Zantac, Рассел вспомнил, что принял тысячи этих таблеток. Он любил играть в американский футбол — тренировки были его хобби. Но сейчас, в 58 лет, он крайне ослаб после перенесенных тревог и операций. Рассел намерен найти виновных; он прочитал о решении федерального судьи в декабре. «Я хотел бы провести день в зале суде, — говорит он, — хотелось бы услышать, что судья скажет мне, откуда, по их мнению, у меня возник рак».
У Джеймса Гетца отказывают почки, и вскоре ему понадобится диализ, но он в состоянии работать и собирается давать показания в зале суда округа Аламеда. Когда Zantac отозвали, у него остались четыре купленных флакона с лекарством. Они хранятся в морозильной камере в офисе одного из его адвокатов, Брента Визнера, как и оставшиеся таблетки Рассела. Тесты показали, сообщает Виснер, что в одной из таблеток, которые принимал Гетц, содержится 3000 нг NDMA; в других таблетках, которые принимал Рассел, этого соединения в два раза больше. Визнер заявил, что пригласил GSK для проведения тестов таблеток, однако представители компании не изъявили желания присутствовать.
Boehringer, Pfizer и Sanofi урегулировали дело Гетца в декабре; сумма компенсации держится в секрете. GSK тоже может договориться с истцом. Если этого не произойдет, Визнер и его партнер по делу Дженнифер Мур будут рассматривать дело в том же суде, где Визнер выиграл процесс на 2 миллиарда долларов против Bayer AG от имени семейной пары, которая утверждала, что гербицид Roundup привел к развитию у них рака. Позже судья уменьшил приговор до 87 миллионов долларов.
Мур также добилась значительных вердиктов суда, касаемо ее клиентов, в ходе судебного процесса с Roundup. Она сообщает, что научный консенсус относительно канцерогенности гербицида отсутствует, в то время как NDMA признан опасным. Она продолжает, что каждая научная организация, каждое регулирующее агентство говорят, что NDMA является канцерогеном для человека. «И вот у нас в качестве доказательств есть таблетки наших подзащитных, в которой просто астрономические значения канцерогена».
Процесс Гетца имеет особое значение, как первый после решения федерального суда во Флориде. Тогда в компании и среди инвесторов возникло ощущение, что опасность миновала. Исполнительный директор GSK Эмма Уолмсли во время телеконференции 1 февраля [2023 г.] заявила, что все в компании были в восторге от результата.
По словам представителей GSK, проведенный Розенберг обзор 13 эпидемиологических исследований не выявил связи между ранитидином и риском развития какого-либо рака. Однако это не совсем так: судья Розенберг проанализировала 11 исследований, и в четырех из них была выявлена связь, которая, по мнению ученых, заслуживает дальнейшего изучения. Во многих исследованиях, которые оценивала Розенберг, изучался общий риск развития рака. Визнер заявил, что анализ, объединяющий эпидемиологические исследования с данными о раке мочевого пузыря, в том числе и те, что рассматривала Розенберг, демонстрирует статистически значимый повышенный риск в случае приема ранитидина.
Справедливости ради, необходимо отметить, что научные данные не могут быть использованы как 100 %-доказательства в пользу какого-то мнения. И вполне вероятно, что разные судьи и присяжные придут к разным выводам. GSK может столкнуться с многолетними судебными исками в Калифорнии, Делавэре и других штатах с вероятностью возмещения убытков истцам на огромные суммы: от 3,5 до 17 миллиардов долларов. В июле 2020 года представители компании также сообщили, что сотрудничают с расследованием Министерства юстиции относительно Zantac.
Pfizer и Sanofi сталкиваются с аналогичными судебными исками из-за продаж потенциально опасного продукта. Как и GSK, они оспаривают тот факт, что Zantac представляет какую-либо угрозу для здоровья. Когда Pfizer попросили прокомментировать ситуацию, представители компании сослались на заявление на своем веб-сайте, в котором отмечается, что последний раз компания продавала Zantac в 2006 году и что у нее «существуют существенные возражения против настоящего судебного разбирательства, а судам предстоит еще решить серьезные юридические и фактические вопросы». Представитель Sanofi заявил: «Компания по-прежнему уверена в своей защите в этом судебном процессе, учитывая явное отсутствие научной поддержки требований истцов».
Ученые Sanofi провели собственное расследование того, как NDMA образуется в таблетках Zantac, надеясь, что это позволит внести некоторые коррективы в ход процесса, что оно выдержит проверку FDA и позволит вернуть препарат на рынок. Компания назвала собственные усилия по этому вопросу Project Churchill. Это вылилось в нежелательный результат, который привел к беспрецедентному решению. Sanofi не смогла найти приемлемый способ производства Zantac с ингредиентом, благодаря которому удалось бы сохранить его оригинальную формулу, т.е. ранитидин.
Вместо этого в 2021 году компания изменила состав Zantac на фамотидин, активное вещество, содержащееся в другом лекарстве от изжоги, Pepcid. Новый Zantac уже в продается. На своем веб-сайте Sanofi описывает эту форму препарата как «продолжение устоявшейся истории и наследия бренда Zantac».





