Недавнее возникновение штаммов SARS-CoV-2 H69/V70 [1, 2], D796H [3] и D614G [4] в Великобритании и штамма N501Y в Южной Африке вызвало опасения относительно их чувствительности к воздействию вакцин. Автор работы привлекает внимание к еще одной проблеме: не окажутся ли такие штаммы неуязвимыми перед диагностическими методами обнаружения? Останется ли у ученых возможность отслеживать распространение заболевания?
С момента открытия ВИЧ вирус SARS-CoV-2, возможно, является самым изучаемым микроорганизмом. По всей планете идет процесс генотипирования вируса, что позволяет получать информацию о его генетическом составе практически в режиме реального времени [5]. Скорость мутации составляет порядка двух нуклеотидов в месяц. Этот показатель заметно ниже по сравнению с такими вирусами, как грипп (скорость мутаций четыре нуклеотида в месяц) или ВИЧ (восемь нуклеотидов в месяц) [6]. Мутации могут препятствовать эффективному обнаружению вируса, так как стратегии диагностики не учитывают изменений вирусного генома.
Ожидается, что фиксируемые мутации коронавируса не повлияют на возможность и эффективность применения вакцин. Однако изменения в последовательностях вирусных нуклеиновых кислот и белков ставят под угрозу возможность использования некоторых диагностических методов in vitro, особенно если наблюдаемая мутация происходит в критически важных областях, например, на сайте связывания праймера или антител при методе ПЦР (в режиме реального времени) или в иммунологических методиках. Кроме того, особое внимание привлечено к диагностическим тестам на основе антител, посредством которых производят оценку наличия и концентрации вирусных белков SARS-CoV-2 в биожидкостях (в основном, в лизате из выделений желез носоглотки, ротоглотки или слюны). Наиболее часто используемые иммунологические методы анализа для обнаружения вирусных белков SARS-CoV-2 включают иммуноферментные анализы (ELISA) и иммунохроматографические методики (LFA, от англ. lateral flow assays). Целевые определяемые соединения при этих анализах — преимущественно шипиковые белки (S) или нуклеокапсид (N), как два наиболее распространенных и иммуногенных вирусных белка, присутствующих в геноме SARS-CoV-2.
S-белок — крайне соблазнительный, с точки зрения диагностики, вирусный антиген. Он обладает высокой иммуногенностью и содержит последовательности, уникальные для SARS-CoV-2 [8]. Тем самым к минимуму сводится потенциальная перекрестная реактивность с последовательностями, существующими в иных известных коронавирусах человека, таких как SARS-CoV, вирус ближневосточного респираторного синдрома (MERS, от англ. Middle Eastern respiratory syndrome) и коронавирусы человека 229E, OC43, HKU-1 и NL63 [9]. Однако использование этого белка связано с определенными рисками. Именно S-белок является тем компонентом вируса, который с большей вероятностью может подвергнуться воздействию мутаций, в особенности тех, которые могут влиять на функции вируса, такие как вероятность инфицирования [10], трансмиссивность [11, 12] и способность инфицировать молодых людей (например, мутация около рецептор-связывающего домена может повлиять на процесс проникновения вириона в клетку-хозяина). По мере возникновения мутаций иммунологические анализы, выявляющие S-белок, выдают большое количество ложноотрицательных результатов, а во время пандемии крайне важно получать наиболее точные диагностические результаты.
Наоборот, существует меньшая вероятность развития точечных мутаций в N-белке, что в меньшей степени повлияет на функцию вируса. Таким образом, лучшей мишенью для диагностики in vitro и разработки вакцины против COVID-19 считается N-белок вследствие хорошей сохранности самой его аминокислотной последовательности, увеличения количества сведений о его генетике и биохимии, а также его сильной иммуногенности [14]. Однако N-белок также не застрахован от мутационной изменчивости, и при диагностике in vitro и разработке вакцин необходимо учитывать потенциальные и неизбежные мутации.
Что касается иммунологических анализов для диагностики in vitro, у анализов, в основе которых лежат методики с использованием поликлональных антител, есть явные преимущества в сравнении с анализами, основанными на обнаружении одного эпитопа при помощи моноклональных антител. Поликлональные антитела, распознающие множественные эпитопы N-белка (на поверхности или внутри него), с большей вероятностью продолжат обнаруживать белок, несмотря на наличие множественных мутаций в целевом определяемом соединении. Когда мутация происходит внутри эпитопа, моноклональное антитело, связывающееся только с этим единственным эпитопом, оказывается неспособным обнаружить вирусный белок. Обнаружение «ускользающего варианта» является одним из нескольких хорошо задокументированных преимуществ поликлональных антител [15].
Что касается появившихся штаммов SARS-CoV-2 — N501Y в Южной Африке
[9], H69/V70 [1,2], D796H [3] и D614G [4], — ни в одном из них не
обнаружено мутаций, которые могли бы препятствовать выявлению
коронавирусного белка N диагностическими поликлональными антителами. С
помощью таких антител удалось распознать даже штамм B.1.1.7 (рис. 1), в
котором были выявлены 17 мутаций.
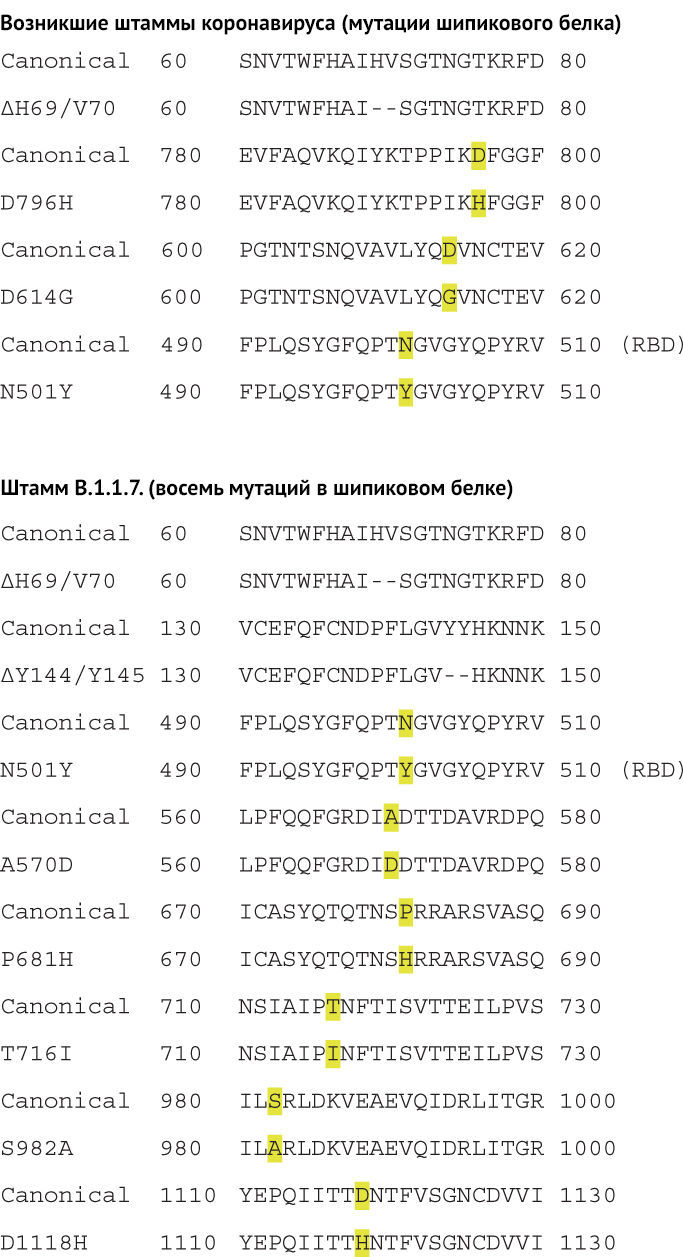
Рисунок 1 | Множество вариантов последовательностей S-белка SARS-CoV-2
Показаны относительные доли последовательностей S-белка. Мутантные позиции в вирусных штаммах обозначены желтым цветом
С учетом этого по мере выявления новых вариантов SARS-CoV-2 крайне необходима регулярная «перенастройка» диагностических методик и тестов. В частности, должна быть повторно подтверждена эффективность тестов против возникающих штаммов коронавируса, диагностической основой которых является использование единственного моноклонального антитела, нацеленного на S-белок. Иной вариант — рассмотреть возможность адаптации диагностической методики к обнаружению N-белка с использованием поликлональных антител высокой аффинности в качестве ключевых реагентов для диагностики.





