В связи с пандемией COVID-19 мировое здравоохранение переживает беспрецедентный всплеск числа тяжелобольных пациентов, которым требуется искусственная вентиляция легких. Необходимость длительной вентиляции легких у тех, кто выживает, означает, что для многих из них может быть рассмотрен вопрос о трахеостомии, чтобы освободить этих пациентов от респираторной поддержки и максимально рационально использовать ограниченные ресурсы. COVID-19 создает особые требования к проведению трахеостомии: медицинские работники должны безопасно осуществлять данную процедуру и контролировать состояние пациентов после нее, минимизируя риски распространения внутрибольничной инфекции и снижения качества медицинской помощи. Существуют противоречивые рекомендации относительно подбора показаний, сроков и техники выполнения трахеостомии, а также последующего ведения пациентов.
В связи с этим авторы организовали международную рабочую группу из лиц, обладающих соответствующими знаниями в области трахеостомии. Авторы провели анализ литературы, в т. ч. и интернет-источников на предмет отчетов о результатах исследований, касающихся трахеостомии во время пандемии COVID-19, а также источников, содержащих рекомендации по уходу за пациентами после данной процедуры. Обобщив опыт стран, которым удалось справиться с резким ростом числа пациентов, новые вирусологические данные, а также международные многопрофильные экспертные заключения по данному вопросу, авторы разработали единые рекомендации по проведению трахеостомии и ведению пациентов после данной процедуры во время пандемии COVID-19.
Введение
Пандемия COVID-19 привела к беспрецедентному увеличению числа пациентов, находящихся в тяжелом состоянии и нуждающихся в искусственной вентиляции легких (ИВЛ). Хотя коронавирус 2 типа, вызывающий тяжелый острый респираторный синдром (SARS-CoV-2), ассоциируется с более низкой смертностью, чем родственные вирусы, вызывающие тяжелый острый респираторный синдром (ТОРС, SARS — severe acute respiratory syndrome — прим. ред.) и Ближневосточный респираторный синдром (БВРС, MERS — Middle East respiratory syndrome — прим. ред.), новый вирус обладает более высокой инфекционностью и скоростью передачи [1]. SARS-CoV-2 распространился гораздо масштабнее и быстрее, чем вышеупомянутые вирусы, что привело к катастрофическим человеческим жертвам во всем мире. Больницы переполнены, а медицинские работники вынуждены принимать трудные решения относительно ухода за пациентами, которые находятся в критическом состоянии. Трахеостомия — это распространенная процедура у тяжелобольных пациентов, которым требуется длительное пребывание на ИВЛ. Использование трахеостомы может облегчить отлучение больного от ИВЛ и потенциально увеличить доступность коек отделений реанимации и интенсивной терапии (ОРИТ). Когда пандемия COVID-19 распространилась на Италию и Испанию, в ОРИТ поступило огромное количество тяжелобольных пациентов, многие из которых нуждались в проведении трахеостомии. Однако трахеостомия — это аэрозоль-генерирующая процедура, поэтому медицинские работники подвергаются риску инфицирования во время ее проведения и последующего ухода за пациентом даже при использовании соответствующих средств индивидуальной защиты (СИЗ).
Аэрозоль-генерирующие процедуры стали ведущей причиной вирусной передачи во время вспышки SARS в 2003 году, причем быстрее всего вирус распространялся в больницах Гонконга, Китая и Канады [2]. Сообщения об инфекциях, связанных с аэрозоль-генерирующими процедурами, появились и в ходе нынешней пандемии [3]. Хотя глобальные общественные стратегии по управлению влиянием COVID-19 являются приоритетными для населения в целом, трахеостомия представляется одним из ряда важных клинических аспектов для оптимального ведения пациентов, находящихся в критическом состоянии, во время пандемии [4]. Авторы предоставляют авторитетные рекомендации для медицинских работников и систем здравоохранения, освещающие широкий круг вопросов, связанных с проведением трахеостомии в период нынешней пандемии COVID-19, путем обобщения имеющихся в настоящее время знаний, доказательств и исторических данных. В связи с острой потребностью в таком руководстве и отсутствием надежных данных о результатах работы ОРИТ авторы дают практические рекомендации, основываясь главным образом на международных многопрофильных экспертных заключениях.
COVID-19 в контексте предыдущих эпидемий
В ответ на угрозу распространения птичьего гриппа, вызванного вирусом гриппа А (H5N1), в 2005 году началась широкомасштабная подготовка к пандемии с целью не только лечения пациентов, но и предотвращения распространения смертельной и легко передаваемой респираторной инфекции. Некоторые из этих методов было бы разумно использовать только в наихудших сценариях, как, например, во время пандемии гриппа 1918–1919 гг., поскольку они являются социально и экономически разрушительными. Гипотеза, лежащая в основе стратегии смягчения последствий для общества, теперь стала широко известна как «сглаживание кривой» (имеется в виду кривая скорости распространения инфекции — прим. ред.) [5]. Благодаря отсрочке пика эпидемии снижается нагрузка на ресурсы системы здравоохранения, а также на больницы и инфраструктуру. Это, в свою очередь, может привести к сокращению общего числа случаев заболевания и негативных последствий для здоровья, что даст больше времени для разработки более эффективных методов лечения и профилактических вакцин.
Оценка этих стратегий в контексте пандемии гриппа 1918–1919 гг. показала, что в городах, принявших данную политику борьбы на ранних этапах, заболеваемость и смертность были значительно ниже, чем в городах, которые ее не придерживались [6]. Поскольку авторы применяют эти стратегии смягчения последствий для общества на глобальном уровне, чего не случалось ранее в истории человечества, последующая оценка определит их влияние на исходы пандемии COVID-19. Трахеостомия была необходимой клинической стратегией для борьбы с эпидемиями 20-го века, связанными с дыхательной недостаточностью, включая полиомиелит и дифтерию [4], и авторы надеются, что внимательное проведение трахеостомии и наблюдение за пациентами после данной процедуры во время нынешней пандемии поможет уменьшить последствия COVID-19.
Методы
Авторы организовали международную рабочую группу для достижения консенсуса по вопросам трахеостомии путем отбора лиц, обладающих соответствующими знаниями в области трахеостомии и опытом разработки рекомендаций или консенсусных документов. Группа имеет международное многопрофильное представительство, включая реаниматологов, анестезиологов, пульмонологов, отоларингологов, медицинских сестер, физиотерапевтов, логопедов, вирусологов и иммунологов, специалистов по медицинской этике и анамнезу, а также заинтересованных лиц из числа пациентов и членов их семей. Масштаб проекта был определен путем пересмотра имеющихся консенсусных утверждений по уходу за пациентами после трахеостомии. Авторы провели литературный и интернет-поиск для выявления и извлечения информации из первоисточников, а также собрали из первых рук данные о трахеостомии во время текущей пандемии в ходе обсуждений среди членов рабочих групп.
Авторы собрали дополнительную информацию путем распространения адресных вопросов и форм для сбора данных, а также опроса Qualtrics-XM (SAP Walldorf, Германия), который позволил членам рабочей группы ранжировать, оценивать и представлять ответы в свободной форме (опрос зарегистрирован в Институциональном Наблюдательном Совете в соответствии с институциональной политикой Мичиганского университета [HUM00182021]). В настоящем документе рекомендации рабочей группы представляют собой экспертное мнение (на протяжении всего документа обозначаемые словами «авторы предлагают»), исходящее из наилучших имеющихся данных, или опубликованные обосновывающие заявления (обозначаемые словами «авторы рекомендуют»). Чтобы определить приоритетность тем для включения и достичь консенсуса в отношении рекомендаций, авторы использовали адаптированный из метода Дельфи итеративный подход. Первый этап состоял из подготовки основным коллективом авторов четких утверждений в рамках данного документа, включающих рекомендации по выбору клинических случаев, срокам, выполнению трахеостомии и ведению пациентов после процедуры на основе полученных из первоисточников данных.
Эти рекомендации были распространены среди всех членов рабочей группы с просьбой как высказать личное мнение, так и предоставить любые дополнительные рекомендации. Второй этап включал распространение между членами рабочей группы полученных новых рекомендаций, а также рекомендаций из первого этапа, удостоившихся положительных комментариев от большинства (более чем половины) респондентов. Окончательный обзор рекомендаций проводился в ходе видеоконференции, в которой приняли участие 29 членов рабочей группы, после чего происходили электронная переписка и телефонные обсуждения, облегчающие повторный обзор и уточнения по всем трем этапам для достижения единого согласия в отношении содержания данного документа.
Отбор пациентов для трахеостомии
Сначала авторы рассмотрели роль трахеостомии у пациентов, находящихся в критическом состоянии и имеющих дыхательную недостаточность. Примерно 8–13 % пациентов, госпитализированных в современные ОРИТ и нуждающихся в ИВЛ, выполнена трахеостомия [7]. Основным показанием к трахеостомии остается облегчение механической вентиляции в течение длительного периода времени, при этом минимизируются осложнения, связанные с наличием эндотрахеальной трубки и отлучением от вентиляции. Трахеостомия может также потребоваться при фактической или угрожающей обструкции дыхательных путей, отеке гортани (который может быть новым признаком COVID-19) [8] или неудачной экстубации из-за слабости, слабого кашля, вязких выделений или комбинации этих факторов. Принятие решений об интенсивной терапии и трахеостомии во время пандемии COVID-19 основывается главным образом на существующих стандартах лечения, хотя доказательная база для определения сроков проведения трахеостомии у тех, кто находится в критическом состоянии, не является существенной [9]. Трахеостомия в контексте критического состояния не всегда отвечает интересам пациента.
Среди пациентов без COVID-19, которым требуется трахеостомия после длительного периода ИВЛ, по крайней мере половина не живут более 1 года, и менее 12 % в течение 1 года находятся дома и являются функционально независимыми [10]. Для пациентов с COVID-19 трахеостомия тоже не всегда может быть полезной. Помимо того, данная процедура и последующее лечение подвергают медицинских работников повышенному риску заражения SARS-CoV-2. Пациенты и их представители нуждаются в информировании и обсуждении в рамках многопрофильной группы компромиссов, проблем и исходов трахеостомии; следует объяснять, что трахеостомия в этом контексте будет часто сопровождаться длительными периодами функциональной зависимости и реабилитации. Эти решения могут стать более важными в условиях перегруженности системы здравоохранения, не располагающей достаточными ресурсами для ухода за пациентами, находящимися в критическом состоянии, выздоравливающими или функционально зависимыми. Хотя нормирование в здравоохранении не является чем-то беспрецедентным, в современную эпоху авторы еще не сталкивались с перспективой нормирования медицинских товаров и услуг в таких больших масштабах. Лицам, ответственным за принятие решений, возможно, придется рассмотреть вопрос о целесообразности проведения трахеостомии с использованием соответствующих медицинских ресурсов в условиях нехватки персонала, оборудования, медикаментов и медицинских учреждений. Независимый комитет по медицинской сортировке или этике мог бы помочь в принятии решений, общении с пациентами и их родственниками, а также уменьшить нагрузку на персонал, находящийся на передовой борьбы с заболеванием [11].
Сроки проведения трахеостомии
Актуальные вирусологические данные
Систематический обзор, в котором сравнивались медицинские работники, проводившие во время вспышки SARS в 2003 году аэрозоль-генерирующие процедуры, с теми, кто не проводил их, выявил повышенный риск заражения SARS у тех, кто проводил интубацию трахеи (отношение шансов 6,6 [95 % ДИ 2,3–18,9]) и трахеостомию (4,2 [1,5–11,5]), а также у тех, кто назначал пациентам неинвазивную вентиляцию легких (3,1 [1,4–6,8]) и проводил ручную вентиляцию перед интубацией (2,8 [1,3–6,4]) [2]. Хотя данные об инфекционности SARS-CoV-2 являются скромными, сообщалось о случаях инфицирования и смерти среди медицинских работников [3, 12]. Среднее время от момента заражения SARS-CoV-2 до появления симптомов (инкубационный период) составляет приблизительно 5 дней (диапазон от 4 до 14 дней) [13,14]. Наибольшее содержание SARS-CoV-2 в организме приходится, как правило, на период возникновения симптомов, что определяется методом ПЦР с вирусной РНК из образцов слизистой оболочки верхних дыхательных путей. После появления симптомов вирусная нагрузка обычно снижается в течение следующих 3–4 дней [15]. У большинства пациентов образцы из нижних дыхательных путей оставались ПЦР-положительными в отношении SARS-CoV-2 до 39 дней после того, как образцы из верхних дыхательных путей становились ПЦР-отрицательными [16].
У пациентов с тяжелым течением заболевания нагрузка вирусной РНК значительно выше и снижается медленнее, чем у пациентов с легким течением [17,18]. Иммунный ответ (противовирусные антитела) обычно возникает как в выделениях дыхательных путей, так и в крови примерно через 7 дней после появления симптомов, а к 12-му дню после их появления обнаруживается у 90 % пациентов [17]. Наличие антител подавляет инфекционность обнаруживаемого вируса. Наличие вирусной РНК, обнаруженной методом ПЦР (так называемое вирусовыделение), не обязательно указывает на инфекционность, особенно при наличии противовирусных антител. Истинная инфекционность может быть оценена с помощью культивирования вируса в клетках in vitro или выведена из клинических или эпидемиологических данных. Детальный анализ девяти человек, у которых развился COVID-19, установил культуру репликации вируса на нескольких анатомических участках [19].
Содержание вирусной РНК, полученной из глотки, вышло на пик в течение первой недели симптомов, достигнув 7×10⁸ копий в мазке из горла на 4-й день, и сохранялось на протяжении всего периода проявления симптомов и после него. При культивировании инфекционный вирус был обнаружен в образцах из горла и легких, но отсутствовал в образцах стула (несмотря на высокую концентрацию вирусной РНК в фекалиях); патогенный вирус ни разу не обнаруживался в крови или моче. Сывороточные антитела были обнаружены через 7 дней у половины пациентов, а к 14 дню — у всех. Все пациенты переносили заболевание в легкой форме. Авторы этого исследования предсказали незначительный остаточный риск инфекционности спустя 10 дней после появления симптомов, когда у пациента было менее 100 000 копий вирусной РНК на 1 мл мокроты [19]. На рисунке 1 показана хронология типичного клинического течения тяжелой формы инфекции SARS-CoV-2, основанная на локальных данных авторов и опубликованных сериях случаев заболевания [13,17,19–23]. Необходимы дальнейшие исследования для изучения иммунного ответа на SARS-CoV-2 у тяжелобольных пациентов, пациентов с сопутствующими заболеваниями и ослабленным иммунитетом, а также для установления вирусной нагрузки, которую создают у этих пациентов различные аэрозоль-генерирующие процедуры.
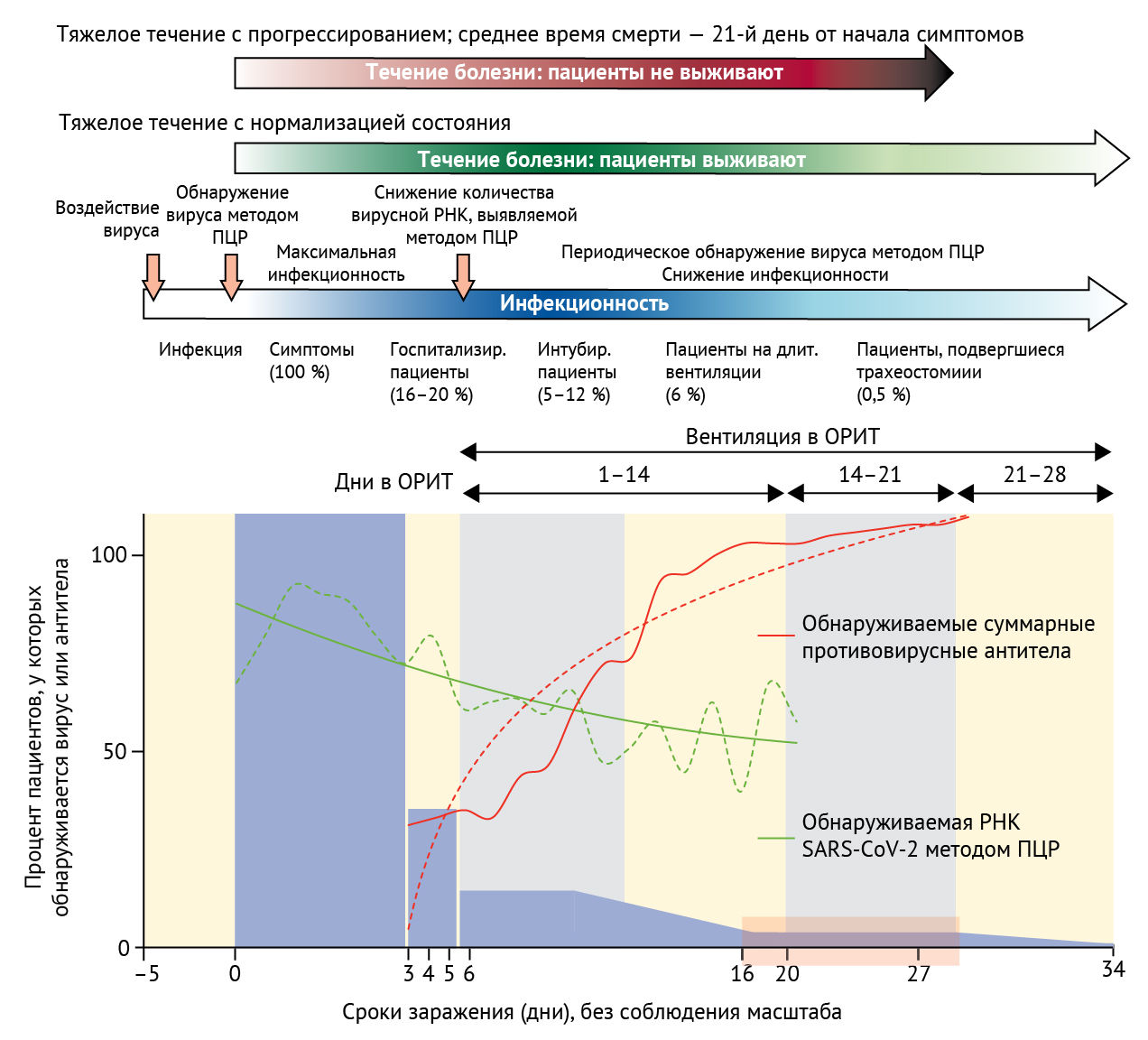
Рисунок 1 | Типичное клиническое течение, ПЦР-диагностика, обнаружение противовирусных антител и инфекционность тяжело протекающей SARS-CoV-2 инфекцииПрозрачный красный прямоугольник показывает предлагаемое окно для проведения трахеостомии — на 10–21-й день пребывания в ОРИТ, что соответствует 16–30-му дню от начала проявления симптомов. Сплошные кривые и столбцы отражают долю всех случаев. Ноль на шкале времени — это начало проявления симптомов (значения по оси Х указаны без соблюдения масштаба). Данные временной шкалы взяты из локальных данных авторов и опубликованных серий случаев [13, 17, 19–22]. Для получения стилизованных кривых были использованы объединенные данные двух исследований, описывающих обнаружение SARS-CoV-2 методом ПЦР и обнаружение противовирусных антител [16, 18]. Объединенные данные по вирусу и антителам включали 181 пациента, из которых 32 (18 %) были определены как находящиеся в критическом состоянии, а 72 (40 %) — как тяжелобольные на основании совпадающих серий случаев [17]. Эти данные репрезентативны для популяции, представляющей интерес, 16–20 % из которой, вероятно, нуждаются в госпитализации в ОРИТ [19]. ОРИТ = отделение реанимации и интенсивной терапии. SARS-CoV-2 = коронавирус 2 типа, вызывающий тяжелый острый респираторный синдром.
Проведение трахеостомии во время пандемии COVID-19
Вне контекста пандемии COVID-19 существуют споры о сроках проведения трахеостомии [24,25]. Хотя некоторые рекомендации поддерживают раннюю трахеостомию у отдельных групп пациентов, например, с черепно-мозговой травмой и с травматическими повреждениями в целом, показания к проведению трахеостомии чаще всего определяются индивидуально [26,27]. Отсрочка трахеостомии у пациентов с COVID-19 может снизить риск для персонала, однако увеличение продолжительности интубации, седации, ИВЛ и связанное с этим пребывание в ОРИТ могут привести к осложнениям. Авторы предлагают, чтобы принятие решений во время пандемии COVID-19 отражало ряд применимых соображений (рис. 2).
Отбор пациентов для попытки первичной экстубации должен основываться на устоявшейся практике, т. е. она должна проводиться, если у пациента улучшаются сердечно-сосудистые и респираторные физиологические показатели, снижаются маркеры инфекции и воспаления, а также успешно проводится тест спонтанного дыхания [28]. Однако преждевременная экстубация подвергает пациентов и персонал риску, связанному со стратегиями срочной спасательной оксигенации и с повторной интубацией. Авторы рекомендуют применять консервативный подход к попыткам экстубации, ограничиваясь пациентами, которые имеют высокие шансы на успех. При рассмотрении вопроса трахеостомии во время пандемии COVID-19 следует и далее уделять особое внимание современной передовой практике. При выполнении плановой трахеостомии надутая манжета трахеостомической трубки, через которую может осуществляться вентиляция с поддержкой давлением (PSV, pressure support ventilation — прим. ред.), обеспечивает замкнутую систему для контролируемого отлучения от респираторной поддержки. Хотя трахеостомия связана с риском передачи инфекции, стратегия первичной экстубации у пациентов, для которых вероятность успеха невелика, также несет в себе риск.
Несколько членов рабочей группы лично участвовали в проведении сложных повторных интубаций у пациентов с COVID-19 или осведомлены о них, что предполагает определенную роль в снижении риска срочной или экстренной повторной интубации в трудных обстоятельствах. Необходимы данные для понимания сопутствующих рисков инфекционного воздействия на персонал и других пациентов. Методы лечения при неудачной экстубации, такие как высокопоточная оксигенация, CPAP-терапия или неинвазивная вентиляция легких, в различной степени создают опасные аэрозоли и могут быть нецелесообразными; они также ограничивают способность больничных палат подавать кислород [29]. Выздоравливающие пациенты, которым по-прежнему необходима респираторная поддержка с помощью трахеостомии, могут наблюдаться под минимальной седацией, что упрощает уход за ними и облегчает их перевод в учреждения для терапии менее острых состояний и создает возможности для лечения тяжелобольных пациентов. Хотя при тщательном отборе трахеостомия полезна для пациентов, выздоравливающих после COVID-19-ассоциированного пневмонита, авторы не рекомендуют эту процедуру выздоравливающим пациентам, которые все еще нуждаются в высокой фракционной концентрации кислорода во вдыхаемом воздухе (FiO2), имеют высокие требования к вентиляции и могут нуждаться в переведении в прон-позицию (укладывание на живот — прим. ред.) как части стратегии ИВЛ.
Пациенты с трахеостомой могут располагаться в прон-позиции, но в этом случае теряется визуальный контроль за трахеостомической трубкой, при этом увеличивается риск ее смещения и развития пролежней. Для выздоравливающих пациентов важное значение имеет четкое принятие решений с вариантами, включающими первичную экстубацию с планированием повторной интубации или без него, трахеостомию или, в некоторых случаях, паллиативную помощь. Обеспечение адекватными СИЗ в целях поддержания безопасности медицинских работников является одной из главных задач при принятии решений по ведению пациентов с COVID-19 в ОРИТ. Примечательно, что COVID-19-ассоциированный острый респираторный дистресс-синдром (ОРДС) может характеризоваться повреждением сосудов и нарушением сосудистой регуляции, что может влиять на стратегию оказания неотложной помощи, и необходимость в трахеостомии может быть снижена с помощью высококачественной помощи в ОРИТ, учитывающей характерную патофизиологию [30]. Основываясь на серии клинических случаев и мнении экспертов, авторы предлагают откладывать трахеостомию, по крайней мере, до 10-го дня ИВЛ и
рассматривать ее только тогда, когда у пациентов появляются признаки клинического улучшения.
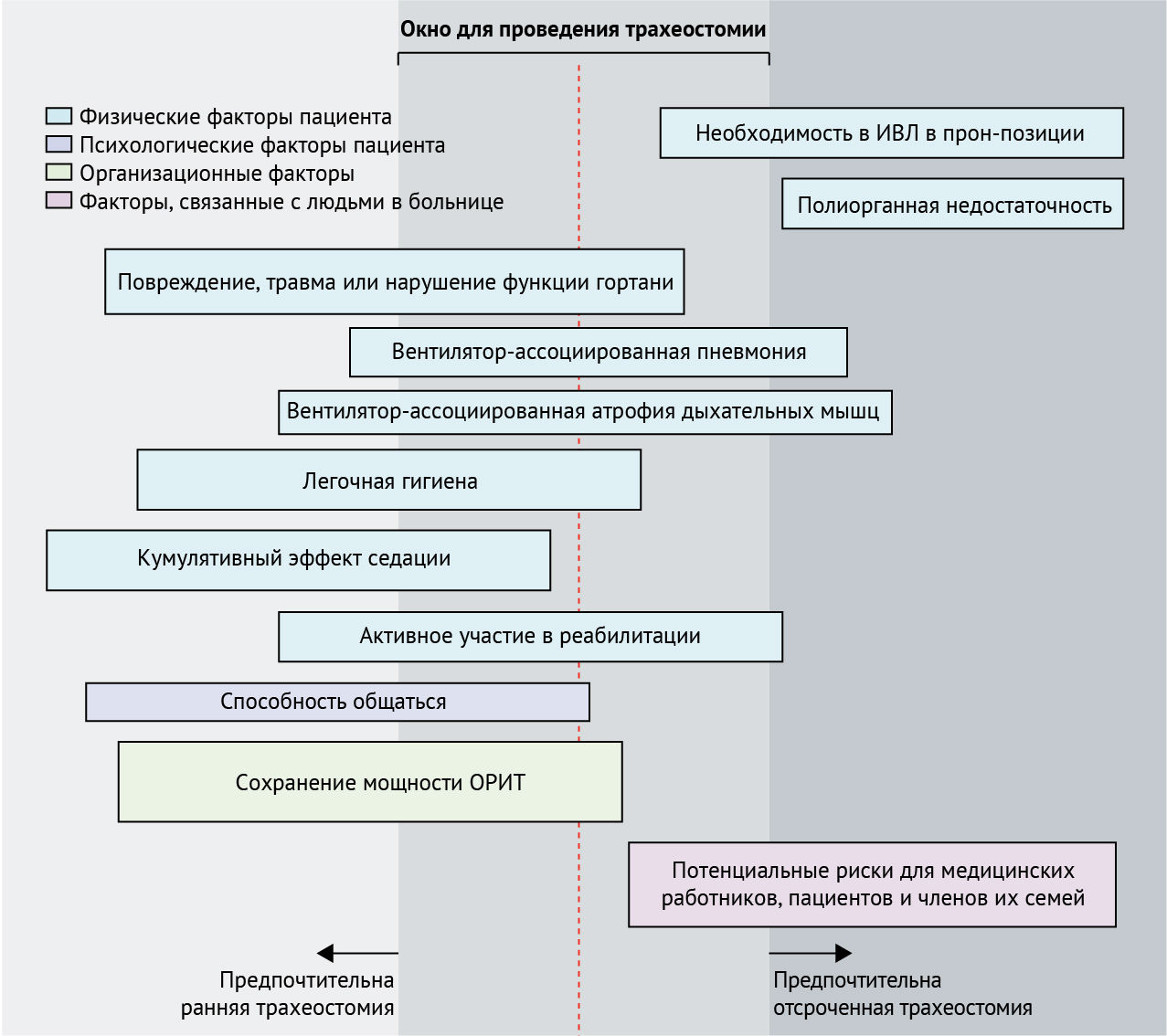
Рисунок 2 | Рекомендация по проведению трахеостомии после интубации при COVID-19-ассоциированном пневмонитеОкно для проведения трахеостомии составляет 10–21-й день после интубации. Высота прямоугольных окон отражает относительную значимость факторов. Высота и расположение окон были предложены и согласованы рабочей группой. ОРИТ — отделение реанимации и интенсивной терапии.
Оптимальные условия для установки трахеостомы
На выбор оптимального места проведения процедуры трахеостомии у пациентов в критическом состоянии влияют различные логистические и практические факторы, такие как подготовка и опыт хирурга, больничная инфраструктура, в том числе обеспеченность палатами для временной изоляции пациентов и возможность создания отрицательного давления в помещении, наличие персонала и оборудования, а также возможность перевода пациента, находящегося в критическом состоянии, в другое место [31]. Трахеостомия может быть выполнена в ОРИТ (часто с неоптимальным оборудованием и освещением, ограниченным количеством ассистентов и неоптимальным размещением на специализированных кроватях) или в операционной (что подразумевает необходимость перевода из ОРИТ, повышенный риск заражения медицинского персонала и необходимость грамотной логистики). Чрескожный, хирургический или комбинированный доступы могут быть использованы в любом из этих мест. Поскольку трахеостомия — это аэрозоль-генерирующая процедура [2], авторы рекомендуют иерархический подход к выбору места проведения операции, чтобы сбалансировать риски для пациента и персонала [32], понимая, что во многих медицинских учреждениях отсутствуют помещения с системой отрицательного давления [1]. Приемлемой альтернативой могут быть портативные высокоэффективные системы фильтрации твердых частиц воздуха. Авторы предлагают реанимационным и хирургическим бригадам выбирать оптимальное место для проведения трахеостомии во время пандемии, уравновешивая риски для пациентов и персонала и оценивая местные возможности и опыт [1].
Оптимальный порядок проведения трахеостомии
Медицинские работники, выполняющие трахеостомию, должны учитывать дополнительные обстоятельства, связанные с инфекционностью SARS-CoV-2. Из опубликованных случаев проведения трахеостомий в Сингапуре, Гонконге и Канаде во время вспышки SARS известно, что больницы использовали усовершенствованные СИЗ в дополнение к стандартным, начиная от защитных экранов для лица и заканчивая электроприводными воздухоочистительными респираторами (PAPR) [1]. На основании этих отчетов авторы предлагают использовать усиленные СИЗ с PAPR, защитой для глаз, водоотталкивающими одноразовыми хирургическими халатами и перчатками. Если PAPR отсутствуют, авторы рекомендуют использовать проверенные на соответствие фильтрующие респираторы 3 класса защиты (FFP3) или маски N95 с дополнительной защитой от жидкости. Количество присутствующего персонала должно быть сведено к абсолютному минимуму, обязательно присутствие наиболее опытных хирурга и анестезиолога. Члены медицинской бригады должны готовиться, тренироваться, симулировать проведение процедуры и эффективно взаимодействовать друг с другом. Техника проведения трахеостомии определяется на основании местного опыта и имеющихся ресурсов. Авторы рекомендуют хирургам продолжать проводить трахеостомию с использованием тех методов и оборудования, к которым они привыкли, в применении которых они уверены и имеют достаточный опыт. Хорошо документированы стратегии по минимизации образования аэрозолей [1].
Чрескожная трахеостомия обычно сопряжена с более частым открытием дыхательного контура аппарата ИВЛ, чем хирургическая трахеостомия, и хотя ультразвуковой и бронхоскопический контроль может повысить безопасность, вероятность образования аэрозоля при чрескожной трахеостомии выше, чем при хирургических подходах. Во время вспышки SARS хирургическая трахеостомия была в целом предпочтительнее, чем чрескожная [33, 34], однако впоследствии чрескожные методы усовершенствовались, и на сегодняшний день нет данных, позволяющих установить превосходство одного подхода над другим с точки зрения инфекционной передачи или безопасности. При выполнении чрескожной трахеостомии предпочтительно использование одноразовых бронхоскопов и закрытых дыхательных контуров аппаратов ИВЛ.
При проведении хирургической трахеостомии авторы предлагают сохранение бескровного поля, минимальное использование диатермии и использование эвакуатора дыма. Не существует однозначных доказательств относительного превосходства какого-либо метода в минимизации инфекционности или осложнений у пациентов, получающих антикоагулянты, в том числе находящихся на экстракорпоральной мембранной оксигенации [35]. Какой бы метод ни использовался, тщательный выбор трахеостомической трубки и тщательная оценка ее положения после установки необходимы для минимизации риска последующего смещения, особенно у пациентов с ожирением [36]. Паралич, возникающий после применения нервно-мышечных блокаторов, устраняет движение и кашель, но у пациентов, находящихся в критическом состоянии, в ответ на такие препараты может возникать тахифилаксия [37,38]. Нервно-мышечный мониторинг (например, TOF-мониторинг — прим. ред.) полезен для обеспечения адекватного уровня плегии во время трахеостомии. Приостановка вентиляции с положительным давлением во время введения трахеостомической трубки минимизирует распространение аэрозоля. Дополнительные манипуляции, такие как размещение надутой манжеты эндотрахеальной трубки значительно ниже места трахеостомии при хирургическом методе, могут свести к минимуму продолжительность апноэ.
Поскольку апноэ может вызвать быструю и значительную гипоксию у пациентов, находящихся в критическом состоянии и зависящих от ИВЛ, авторы предлагают перед проведением трахеостомии использовать у пациента, находящегося в супин-позиции (положении лежа на спине — прим. ред.), преоксигенацию с FiO2 равной 1,0 и положительным конечным давлением в конце выдоха (ПДКВ, PEEP — прим. ред.) равным 5 см вод.ст. с последующей пробой с апноэ в ОРИТ. Быстрое падение сатурации во время этой пробы предсказывает аналогичную реакцию во время проведения трахеостомии, указывая на риск для пациента (а также для персонала, который может потребоваться для выполнения незапланированных или дополнительных вмешательств на дыхательных путях), и в этом случае трахеостомию следует отложить (рекомендация по проведению пробы с апноэ сомнительна и вряд ли применима в реальной клинической практике, т. к. проведение этой пробы будет являться потерей времени, особенно у релаксированных пациентов; необходима только преоксигенация — прим. ред.). Способность проводить или переносить пробу с апноэ не должна заменять междисциплинарное клиническое заключение относительно рисков и преимуществ проведения трахеостомии у конкретного пациента.
Оптимальный уход за пациентом после трахеостомии
Уход за пациентами с COVID-19 после трахеостомии соответствует тем же фундаментальным принципам ухода, которые применяются ко всем пациентам, перенесшим эту процедуру. Безопасный и качественный уход может быть обеспечен в различных условиях [39,40]. Однако из-за риска передачи вируса концепция пациент-ориентированного ухода должна быть сбалансирована с безопасностью для медицинских работников. Пациенты должны быть под наблюдением у опытного персонала, который обучен ведению пациентов с трахеостомой и уходу за ними [41]. Ключевые принципы включают уделение внимания необходимому уходу, недопущение ненужных вмешательств (особенно аэрозоль-генерирующих), раннее распознавание ухудшения состояния и своевременное реагирование на экстренные ситуации. Вмешательства в дыхательные пути следует планировать заранее, насколько это возможно, чтобы можно было использовать соответствующие СИЗ.
Использование СИЗ персоналом остается приоритетным даже в экстренных ситуациях, и авторы предлагают подготовить систему для вызова помощи медицинских работников из смежных клинических сфер деятельности, в которых персонал может уже носить СИЗ. Следует придерживаться стандартных подходов к ведению экстренных случаев трахеостомии. Для пациентов, которые не болеют COVID-19 и имеют трахеостому, риск заражения SARS-CoV-2 от посетителей и персонала неизвестен. Необходимо определить безопасные места для лечения пациентов с COVID-19 и пациентов без COVID-19 с различными потребностями в уходе, и, возможно, потребуется рассмотреть новые варианты, выходящие за рамки стандартных условий больничных палат, такие как максимизация использования телемедицины там, где это применимо. Трахеостомия с целью облегчения длительного периода респираторной поддержки или отлучения от аппарата ИВЛ первоначально требует замкнутой системы для подачи давления в легкие. Стратегии, направленные на минимизацию отсоединений дыхательного контура и рисков вдыхания аэрозоля персоналом, включают использование нефенестрированной трахеостомической трубки с манжетой, использование закрытых всасывающих катетеров и уклонение от ненужных вмешательств на дыхательных путях [42,43]. Манжеты должны оставаться первоначально надутыми, а давление следует проверять каждые 12 ч и поддерживать на уровне 20–30 см вод.ст. или выше пикового давления вдоха (PIP, peak inflation pressure — прим. ред.). Следует избегать использования заполненных водой трахеостомических трубок с манжетами и многократного проведения тестов на герметичность (для предотвращения аэрозолизации), если только персонал не экипирован СИЗ полностью [44]. Замена трубок должна быть отложена в идеале до тех пор, пока пациенты не перестанут считаться инфекционными [43].
Увлажнение и использование одноразовых внутренних канюль являются распространенными стратегиями защиты от закупорки трубок выделениями дыхательных путей и снижения требований к отсасыванию [45]. В случае использования внутренней канюли авторы предлагают уменьшить частоту ее замены и ежедневно оценивать ситуацию. Авторы рекомендуют использовать простой тепло- и влагообменный фильтр (HME), который обеспечивает адекватное увлажнение и не создает аэрозолей [46]. Активное увлажнение на водной основе может потребоваться, если выделения густые, но его использование должно оцениваться индивидуально. Небулайзеры могут улучшить выведение секрета, но требуют дополнительной обработки дыхательных контуров и могут забивать фильтры HME, поэтому их следует использовать только после тщательного обсуждения (https://medach.pro/post/2380; https://medach.pro/post/2303). Отлучение от ИВЛ, как правило, осуществляется путем постепенного снижения поддержки давлением, периодического сдувания манжеты, использования методов вокализации, стимулирования кашля и восстановления глотания. Многие из этих мероприятий включают в себя создание дополнительных воздушных потоков, проходящих через голосовые связки, в том числе «регулируемая вентилятором “утечка” речи» (VALS, ventilator-adjusted leak speech: https://youtu.be/8CnM2C0td7A); во время проведения ИВЛ манжета трахеостомы раздута, что препятствует утечке воздуха и создает герметичность дыхательного контура; при сдувании манжеты часть воздуха во время выдоха может проходить выше стояния трахеостомы через голосовые связки, что, в свою очередь, создает возможность общаться с пациентом — т. н. «утечка» речи; одновременно с этим, возникающая «утечка» идентифицируется респиратором как сигнал опасности, поэтому с целью компенсации «утечки» стоит увеличить скорость воздушного потока или добавить PEEP (ПДКВ); это теоретически может улучшить коммуникацию с пациентом — прим. ред.), стратегии манжетной вокализации (ACV, above-cuff vocalisation: https://youtu.be/IAcfufLvM-c); часть данной методики схожа с вышеописанной, т. е. основана на утечке воздуха выше стояния трахеостомической трубки при спущенной манжете; однако, в сравнении с методикой VALS, при проведении ACV нет респиратора; стоит сказать о том, что существует несколько вариантов трахеостомических трубок: с манжетой, без манжеты, с фенестрацией, без фенестрации; в данном случае наличие в трахеостомической трубке дополнительного отверстия способствует увеличению воздушного потока на выдохе, «убегающего» выше уровня стояния трахеостомической трубки к голосовым связкам, что в свою очередь улучшает вокализацию пациента; особенно полезна данная методика для пациентов с поврежденными верхними дыхательными путями, но способных дышать, а также разговаривать, самостоятельно — прим. ред.) и использование речевых клапанов [47]. Возможность образования аэрозоля у пациента с трахеостомой и сдутой манжетой, находящегося на вентиляции с положительным давлением, вероятно, аналогична такой возможности у пациента на CPAP-терапии, хотя различные аппараты ИВЛ генерируют различные максимальные потоки [2].
Авторы предлагают пациентам использовать маски и лицевые щитки, чтобы уменьшить риски, связанные с распространением аэрозоля. Чрезмерно осторожный подход может поставить пациентов в невыгодное положение, замедляя их выздоровление и ограничивая их способность общаться. Для уменьшения потенциального чувства изолированности у пациентов и повышения безопасности во время пандемии COVID-19 необходимо применять творческие методы альтернативной аугментативной коммуникации [48]. Инфекционные пациенты, которые клинически готовы начать попытки сдувания манжеты, должны наблюдаться в местах, предназначенных для лечения пациентов с COVID-19, опытным персоналом, который защищен соответствующими СИЗ. Оценка глотания должна опираться на клинические навыки, а не на использование инструментальных методов исследования. Деканюляция должна рассматриваться так скоро, насколько это возможно и безопасно, и контролироваться многопрофильной командой специалистов в области трахеостомии.
Обобщение рекомендаций по трахеостомии во время пандемии COVID-19
Трахеостомия по-прежнему играет важную роль в контроле отлучения от длительных периодов ИВЛ во время пандемии COVID-19, но эта процедура не всегда может принести пользу, и ее проведение и последующий уход за пациентами представляют опасность для медицинских работников. Рекомендации рабочей группы представляют собой экспертные мнения (обозначаемые словами «авторы предлагают» на протяжении всего текста), основанные на наилучших имеющихся доказательствах, или опубликованные обосновывающие заявления (обозначаемые словами «авторы рекомендуют»).
Отбор пациентов для проведения трахеостомии
• Авторы предлагают адаптировать стандартное принятие решений к пандемии COVID-19, принимая во внимание целый ряд соображений, включая потенциальные риски и пользу для каждого пациента, риски для медицинских работников, других пациентов и членов их семей, а также имеющиеся ресурсы здравоохранения.
Сроки проведения трахеостомии
• Авторы предлагают отложить трахеостомию по крайней мере до 10-го дня ИВЛ и рассматривать ее только тогда, когда у пациентов появляются признаки клинического улучшения.
• Авторы рекомендуют применять консервативный подход к попыткам экстубации, ограничиваясь пациентами, у которых прогнозируется высокий шанс на успех.
Выполнение трахеостомии
• Авторы предлагают реанимационным и хирургическим бригадам рассматривать оптимальное место для проведения трахеостомии во время пандемии, уравновешивая риски для пациентов и персонала и принимая во внимание местные возможности и опыт.
• Авторы рекомендуют применять иерархический подход к выбору места проведения операции, уравновешивая риски для пациента и персонала.
• Авторы предлагают использовать усиленные СИЗ, в том числе PAPR, средства защиты глаз, водоотталкивающие одноразовые хирургические халаты и перчатки.
• Авторы предлагают хирургам продолжать делать трахеостомию с использованием тех техник и оборудования, с которыми они знакомы, в применении которых они уверены и имеют достаточный опыт.
• Авторы предлагают сохранение бескровного поля, минимальное использование диатермии и использование эвакуатора дыма при проведении хирургической трахеостомии.
• Авторы предлагают перед проведением трахеостомии использовать у пациента, находящегося в супин-позиции (положении лежа на спине — прим. ред.), преоксигенацию с FiO2 равной 1,0 и положительным конечным давлением в конце выдоха (ПДКВ, PEEP — прим. ред.) равным 5 см вод.ст., с последующей пробой с апноэ в ОРИТ, чтобы показать физиологическую готовность переносить процедуру, а также применять стратегии уменьшения аэрозолизации (рекомендация по проведению пробы с апноэ сомнительна и вряд ли применима к реальной клинической практике, т. к. проведение этой пробы будет являться потерей времени; необходима только преоксигенация — прим. ред.).
Оптимальный уход за пациентом после трахеостомии
• Ключевые принципы включают уделение внимания необходимому уходу, недопущение ненужных вмешательств (особенно аэрозоль-генерирующих), раннее распознавание ухудшения состояния и своевременное реагирование на экстренные ситуации.
• Авторы предлагают подготовить системы для вызова помощи персонала из смежных клинических сфер деятельности во время проведения экстренной трахеостомии (персонал уже может носить СИЗ в рамках подготовки к таким чрезвычайным ситуациям).
• Авторы предлагают уменьшить частоту замены внутренней канюли (если она используется) и проверок давления в манжете; эти решения должны приниматься индивидуально и пересматриваться ежедневно.
• Авторы рекомендуют начинать уход после трахеостомии с простого тепло- и влагообменного фильтра (HME) для обеспечения увлажнения; потребность в увлажнении с подогревом или в дополнительных средствах, таких как использование небулайзера для введения физиологического или гипертонического солевого раствора, должна определяться индивидуально и оцениваться ежедневно.
• Авторы предлагают пациентам, проходящим пробы сдувания манжеты трахеостомической трубки, использовать маски и лицевые щитки, чтобы уменьшить риски, связанные с распространением аэрозоля.
ОРИТ — отделение реанимации и интенсивной терапии. СИЗ — средства индивидуальной защиты. FiO2 — фракционная концентрация кислорода во вдыхаемом воздухе.
Стратегия поиска и критерии отбора
Авторы проводили поиск на PubMed, Embase, MEDLINE и в интернете (Google и Google Scholar из британского интернет-соединения), в том числе в «серой» литературе, статей, опубликованных в период с 1 января по 4 апреля 2020 года, без языковых ограничений, используя комбинации поисковых терминов «коронавирус», «COVID-19», «трахеостомия» и «трахеотомия». Выявленные источники включали утверждения и рекомендации, полученные с веб-сайтов больниц или признанных национальных обществ, определенных стратегией поиска, или известные авторам этой работы, многие из которых либо были вовлечены в разработку национальных, местных или узкоспециализированных руководств, либо осведомлены о них. Когда данные повторялись в нескольких источниках, предпочтение отдавалось источникам, представляющим национальные группы или более крупные серии наблюдений. Окончательный список литературы был составлен на основе соответствия темам, затронутым в настоящем документе, с целью предоставления актуального обзора новых данных по COVID-19, имеющих непосредственное отношение к планированию, проведению трахеостомии и последующему ведению пациентов во время пандемии.
Заключение и дальнейшие направления
Обобщение рекомендаций по применению трахеостомии во время пандемии COVID-19 представлено в информационном окне. Определяющей чертой этой пандемии является ее всепроникающий и изменчивый характер. Увеличение числа пациентов с COVID-19, находящихся в критическом состоянии, может привести к быстрому переполнению больниц, в частности, из-за того, что многим пациентам требуются длительные сроки респираторной поддержки, и многим для облегчения выздоровления потребуется трахеостомия. На глобальном уровне исследования пандемии COVID-19 описывают одну и ту же проблему: прогнозирование и планирование спасают жизни, в то время как недостаточная готовность приводит к перегруженности систем здравоохранения. Поскольку трахеостомия находится на стыке безопасности медицинских работников, распределения ресурсов и пациент-ориентированного ухода, наличие разумного руководства имеет решающее значение. Многие вопросы остаются без ответа, и необходимы перспективные данные для ответа на насущные вопросы, касающиеся трахеостомии в условиях пандемии COVID-19. Данные об инфекционности и персистенции вирусной РНК у пациентов, находящихся в критическом состоянии, ограничены, особенно касаемо сроков, превышающих 20 дней с момента появления симптомов, когда обычно рассматривается трахеостомия.
Прогностическое значение пика вирусной нагрузки и антительного ответа для оценки инфекционности и риска передачи вируса, связанного с различными стратегиями введения трахеостомы, требует дальнейшего изучения. Опыт европейских стран показывает, что готовность является мощным фактором, определяющим результаты лечения пациентов. Отсроченная интубация и нехватка аппаратов ИВЛ приводят к неблагоприятным исходам. Важное значение имеют надежный сбор, анализ и сопоставление данных, как, например, подход, применяемый в рамках Глобального сотрудничества в области трахеостомии (GTC, Global Tracheostomy Collaborative — прим. ред.) [39]. Если в кризисной ситуации используются нетрадиционные подходы к лечению (например, общие аппараты ИВЛ или ранняя трахеостомия), существует моральный долг изучить эти вмешательства для оценки их безопасности и эффективности.
Авторы
BAM, MJB, и SJW внесли вклад в разработку концепции и дизайна работы, сбор, анализ, интерпретацию данных и подготовку рукописи. BAM и MJB выполнили литературный поиск. BAM, MJB, SJW, и PJMO подготовили изображения. VP, RDT, SDB, и GCYL внесли вклад в интерпретацию данных. AA, NT и DJF-K внесли вклад в разработку концепции и дизайн работы, сбор, интерпретацию данных и подготовку рукописи. TSC, SG и AD внесли вклад в сбор, интерпретацию данных и подготовку рукописи. JMA и GHM предоставили данные, внесли вклад в их интерпретацию и подготовку рукописи. CM и CHR предоставили данные и внесли вклад в их интерпретацию. JA, SV, PD, JZ, MA, PP, PJMO и HM внесли вклад в разработку дизайна работы, сбор, интерпретацию данных и подготовку рукописи. LQ предоставил данные и внес вклад в разработку дизайна работы, сбор, интерпретацию данных и подготовку рукописи. BKW и EW внесли вклад в разработку дизайна работы, интерпретацию данных и подготовку рукописи. YS и MS предоставили данные и внесли вклад в интерпретацию данных. Все авторы внесли вклад в критический пересмотр рукописи с точки зрения ее интеллектуального содержания, и все они несут ответственность за содержание настоящего документа.
Декларация конфликта интересов
VP является консультантом компании Medtronic. CHR и DJF-K сообщают о неограниченных грантах от компании Cook Medical, поддерживающей медицинское образование; CHR сообщает о заявке на патент на защитный интубационный тент и способ использования и дезинфекции (заявка на патент США № 63/000, 106, поданная 26 марта 2020 года, и заявка № 63/012, 746, поданная 20 апреля 2020 года; лицензиат — попечители Пенсильванского университета). JA сообщает о гранте от Becton-Dickinson вне рамок представленной работы. JZ сообщает о плате за консультационные услуги от Karl Storz и Zeiss вне рамок представленной работы. MA сообщает о грантах от GE и Intersurgical, а также о личных гонорарах от Orion и Intersurgical вне рамок представленной работы. MS сообщает о гранте от NewB и взносах в его учреждение от Merck Sharp & Dohme, Amormed и Biotest вне рамок представленной работы. Все остальные авторы заявляют об отсутствии конфликта интересов.
Источник: MEDACH





