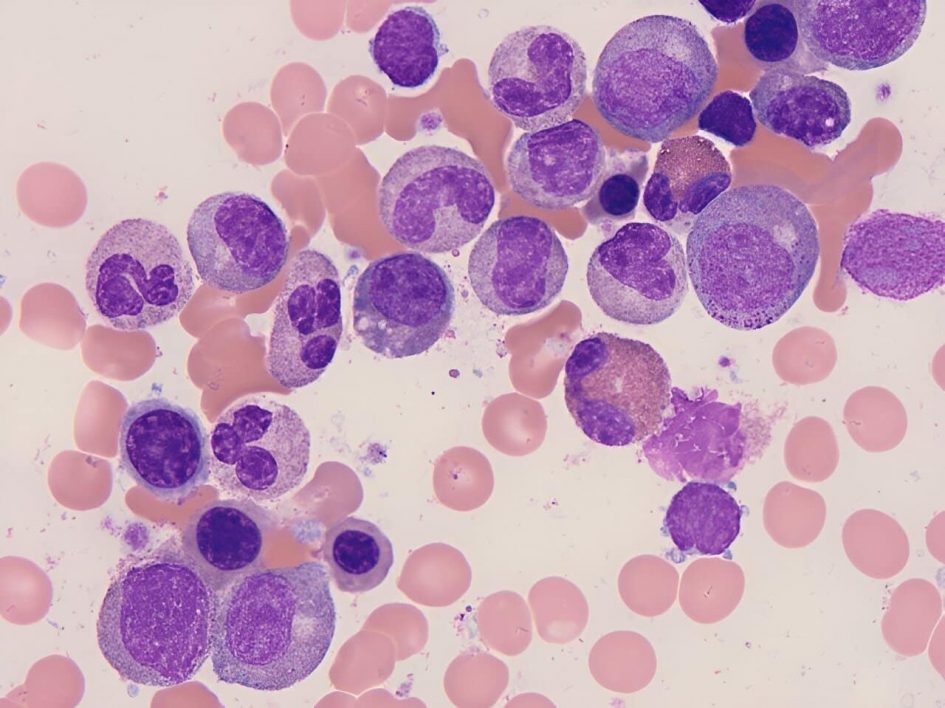
В отличие от большинства клеток с округлыми ядрами нейтрофилы — клетки иммунной системы, которые плавают в нашей крови, — имеют ядра замысловатой дольчатой формы. Благодаря им нейтрофилы способны пробраться туда, куда не проникнут клетки с обычным ядром. Авторы новой статьи в Nature узнали, как образуются такие странные ядра, и предложили использовать этот механизм в качестве нового метода терапии.
Среди клеток крови, которые защищают человека от инфекций, — лейкоцитов — наиболее многочисленны нейтрофилы. Они относятся к так называемому врожденному иммунитету и напрямую участвуют в разрушении (фагоцитозе) непрошеных гостей — различных патогенов вроде бактерий или вирусов.
В отличие от некоторых других форменных элементов крови (зрелых эритроцитов и тромбоцитов) нейтрофилы не лишены ядра, однако его форма очень необычна. Если у большинства клеток ядро круглое или овальное, то у нейтрофилов оно дольчатое, то есть состоит из нескольких соединенных перетяжками сегментов.
Структура ядра заметно отличается у созревающих (палочкоядерных) и зрелых (сегментоядерных) нейтрофилов. Такое необычное видоизменение клеток иммунитета делает их очень подвижными. Нейтрофилы со своим гибким ядром способны «пролезть» через любые ткани — там, где застрянет любая клетка с округлым ядром. Нетрудно догадаться, что их целью при этом служат патогены и места воспаления.
Авторы статьи в ведущем научном журнале Nature выяснили механизмы, благодаря которым нейтрофилы меняют форму своих ядер. Ученые использовали метод избирательного окрашивания клеток и описали изменения конформации (то есть трехмерной формы) хромосом у клеток-предшественниц нейтрофилов.
Оказалось, что в основе уникальной формы ядер — ингибирование механизма упаковки ДНК, который называется «экструзия (или проталкивание) петель» (loop extrusion). В нем участвуют специализированные «молекулярные моторы», в том числе белковый комплекс когезин.
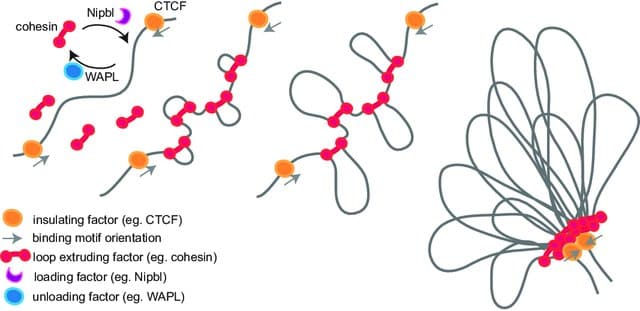
За счет удаления необходимого для экструзии петель фактора NIPBL (nipped-B-like protein) ученые вызвали у клеток — предшественниц нейтрофилов необычные изменения формы ядра: те приобрели форму подковы, ленты, кольца и так далее. Авторы полагают, что это соответствует происходящему с клетками при нормальной дифференциации нейтрофилов, которые таким образом приобретают уникальную архитектуру хроматина и пакуют свои хромосомы в структуры, напоминающие дольки или лепестки. Нехватка NIPBL также остановила деление клеток и «включила» в них специфические гены, которые активны у нейтрофилов.
Авторы надеются, что их результаты имеют не только теоретическое значение и вполне могут стать основой для новых методов терапии. Искусственно придавая ядрам клеток необычную форму, мы сможем улучшить их способность проникать через толщу тканей и, как следствие, эффективнее убивать возбудителей инфекций.