Если вглядеться в них пристально, то станет ясно, что вакцины давно перестали быть тем, чем кажутся.
Пандемия коронавируса SARS‑CoV‑2 заставила нас подтянуть свои знания не только о вирусологии и эпидемиологии, но и о работе иммунной системы. Устоявшееся представление о том, что иммунитет просто защищает организм от внешних угроз, оказалось верным далеко не всегда. Многих жертв COVID‑19 губит не коронавирус как таковой — cмерть приносят собственные лейкоциты больного, которые разрушают ткань лёгкого, отстреливая заражённые клетки, и разводят такую воспалительную панику (так называемый «цитокиновый шторм»), с которой организм справиться не в силах.
Убей другого
Когда в организме заводится чужак, иммунной системе нужно время, чтобы его обнаружить, сообщить о нём в вышестоящие инстанции (лимфатические узлы, костный мозг и селезёнку) и подогнать войска. Гораздо удобней было бы, если бы армия уже находилась в боевой готовности. Для этого и нужна вакцина.
Прививка — это болезнь в миниатюре. Мы заражаем свой организм возбудителем, но он настолько слаб или пассивен, что война иммунитета с ним заканчивается победой в первой же битве, победители не несут потерь и затем переключаются на патрулирование территории.
Но что произойдёт, если противников будет не один, а два — то есть если вскоре после введения вакцины в организм попадет ещё один, другой патоген?
Дело в том, что в самом начале боевых действий в наступление идут солдаты врождённого иммунитета, которые не отличаются большой фантазией. Тактика их боя не зависит от того, кто им достался в противники. Например, противовирусный ответ начинается с интерферонов 1‑го типа — это белки, которые запускают в клетках режим «чрезвычайной ситуации». В таком режиме клетка притормаживает синтез своих ДНК, РНК и белков, чтобы в случае её захвата вирус не мог размножаться. А если так, то совершенно неважно, кто именно атакует организм и сколько их — чрезвычайная ситуация душит любое предприятие.
Поэтому можно предположить, что если в ваш организм попал коронавирус, а вы при этом только что ввели чрезвычайное положение по случаю войны с вакциной, оно если не остановит, то хотя бы притормозит вторжение нового интервента. Исходя из этого, американский вирусолог Константин Чумаков, который занимается оценкой эффективности и безопасности вакцин в FDA (американском минздраве), предложил бороться с коронавирусом с помощью давно изученной ослабленной вакцины от полиомиелита. В этом он наследует своим родителям — русским вирусологам Марине Ворошиловой и Михаилу Чумакову — которые занимались внедрением живой вакцины от полиомиелита в СССР в 50‑х годах ХХ века.
Массовая вакцинация не только позволила за полвека избавиться от двух типов полиовирусов из трёх, но также привела к неожиданным последствиям, напрямую с полиомиелитом не связанным. Например, в 2000‑х годах в африканской Гвинее‑Бисау прививки снизили смертность детей на 19 процентов — и это в те годы, когда полиомиелитом в стране никто не болел. Китайские учёные отметили, что у детей, привитых от полиомиелита, режевозникают инфекционные воспаления во рту и на конечностях. А в России, по словам Чумакова‑младшего, кампания по вакцинации от полиомиелита ещё в 1970‑х годах снизила смертность от сезонного гриппа в четыре раза. И коль скоро вакцина оказалась хорошим подспорьем в борьбе с другими вирусами, почему бы не воспользоваться этим оружием снова?
У вакцины от полиомиелита есть безусловные плюсы: она известна давно, хорошо изучена и стоит недорого. Тем не менее здесь есть некоторые тонкости.
Дело в том, что вакцин от полиомиелита две. Первая это упомянутая живая ослабленная — её детям капают в рот или скармливают на кусочке сахара. А вторая — инактивированная, её вводят в мышцу инъекцией.
Инактивированная появилась раньше: она безопаснее, но и менее эффективна. Родители Константина Чумакова бились за введение живой вакцины, которая даёт более сильный иммунный ответ, и с тех пор во всём мире используют именно её. Но постепенно, по мере избавления от полиовируса, страны начали переходить обратно на инактивированную вакцину, чтобы не подвергать риску людей с ослабленным иммунитетом.
Если сейчас начать снова массово использовать живую вакцину, есть шанс, что люди из группы риска могут пострадать. Поэтому даже для давно знакомой вакцины необходимы тщательные испытания (их собираются проводить, например, в России). И если такой метод встряски иммунитета и станет для кого‑то спасением, то только для тех, кто ещё не болен, и тех, кому необходима экстренная защита, — в первую очередь, врачей.
Иммунитет
Но если идея с вакциной от полиомиелита ещё выглядит интуитивно понятной — в конце концов, средство от одного вируса может быть полезно и от других — то некоторые другие кажутся гораздо более странными.
Например, многие воодушевились, когда нью‑йоркские учёные подсчитали, что в странах с массовой вакцинацией от туберкулёза смертность от коронавируса ниже, чем в тех, где программу вакцинации свернули. Если бы эти результаты подтвердились, это означало бы, что некоторые страны, где туберкулёз не побеждён и вакцинация от него обязательна (например, Россия), могли бы с облегчением выдохнуть: если не туберкулёз, так хотя бы коронавирус пройдёт по касательной.
Но туберкулёз вызывают бактерии — а COVID‑19 вызывают вирусы.
Статью быстро раскритиковали: корреляцию назвали несущественной, а методику — сомнительной (среди прочего, авторы сравнивали страны в зависимости от среднего дохода населения, который не всегда соответствует качеству медицины). А после тель‑авивские медики сравнили смертность от коронавируса среди невакцинированных израильтян и вакцинированных мигрантов и поставили точку в этой истории — смертность у этих групп не различалась. Выдохнуть не получится.
Тем не менее идея сравнить смертность в зависимости от истории прививок родилась не на ровном месте. Подобно вакцине от полиомиелита, которой приписывают способность предотвращать другие вирусные инфекции, у вакцины от туберкулёза тоже то и дело находятся удивительные свойства.
Противотуберкулёзная вакцина — это ослабленный штамм бычьей туберкулёзной палочки, Mycobacterium bovis (она же зовется бациллой Кальметта — Герена, по имени своих изобретателей, отсюда и сокращение БЦЖ, Bacille Calmette‑Guerin). Она родственна человеческой туберкулёзной палочке — M. tuberculosis.
Первое удивительное свойство БЦЖ в том, что от самого туберкулёза она защищает не так уж и хорошо: в некоторых популяциях эффективность её и вовсе стремится к нулю.
Зато БЦЖ успешно предотвращает лепру, которую вызывают другие члены рода микобактерий. Этому эффекту есть объяснение: у родственных бактерий похожие белки на поверхности клетки. И если организм производит антитела, которые хорошо садятся на одну микобактерию, то с какой‑то долей вероятности они прилипнут и на поверхность её родственницы, запуская иммунный ответ.
Этот феномен называют кросс‑реактивностью. И он срабатывает не только для антител, но и для Т‑лимфоцитов, которые внезапно опознают врага в клетках с непривычными молекулами и убивают их — хотя механизм их работы выглядит наоборот, помнить конкретного противника, чтобы напасть на него при первой встрече.
Иммунитет может таким образом «путать» не только родственные бактерии, но и разные вирусы: ВИЧ и гепатит, грипп и вирус Эпштейна — Барр, бактерии и одноклеточные эукариоты (столбняк и токсоплазму) и даже бактерии и вирусы: цитомегаловирус и чумную палочку, ВИЧ и M. tuberculosis.
Это приводит к тому, что у взрослых людей иногда встречаютсяклетки иммунологической памяти, специфичные к патогенам, которыми их хозяева никогда не болели: в том числе ВИЧ, вирусу герпеса и, как недавно оказалось, даже коронавирусу SARS‑CoV‑2.
Так или иначе, многие исследователи обнаруживали у вакцины БЦЖ способность защищать не только от микобактериальных инфекций. Например, в нескольких популяциях она в два‑три раза снизила смертность детей от всех причин. И это едва ли можно списать на противотуберкулёзную защиту: новорождённые им практически не болеют, а значит, вакцина может действовать какими‑то окольными путями. Постепенно у учёных возникло подозрение, что дело здесь и не в кросс‑реактивности — в некоторых случаях «эффект дежавю», который позволяет справиться с никогда не виденным патогеном, работал независимо от Т- и В‑клеток с их антителами. Это означает, что у иммунологической памяти есть и другие, ранее неизвестные механизмы.
Фокусы с памятью
Классический образ иммунной системы человека — это дерево о двух ветвях: врождённый и приобретённый (адаптивный) иммунитет. И если второй у каждого человека свой и сила его ответа зависит от памяти о предыдущих инфекциях, то первый должен быть одинаков у всех здоровых людей.
Тем не менее появляется всё больше свидетельств того, что это не так.
Даже у растений и беспозвоночных животных, которые лишены системы адаптивного иммунитета, время от времени находят признаки иммунологической памяти: комары с каждым разом всё активнее пытаются убить в себе малярийного плазмодия, а иммунитет ракообразных «вспоминает» своих паразитических червей. Известны примеры и того, какие следы вторжение раздражителя оставляет в клетках врождённого иммунитета: макрофагах (пожирателях бактерий и клеточных обломков) и нейтрофилах (главных борцах с бактериями).
Эти эффекты называют памятью врождённого иммунитета или проявлениями «натренированного иммунитета»— в случае БЦЖ тренером, соответственно, выступает вакцина. На память о пробном сражении с туберкулёзом в организме остаются не только готовые к бою с туберкулёзной палочкой Т- и В‑лимфоциты, но и клетки врождённого иммунитета с измененным обменом веществ. Например, некоторые из них начинают выделять больше сигнальных молекул. В них намечаются эпигенетические сдвиги: одни гены «закрываются» от считывания, другие, наоборот, раскручивают, в результате изменяется и набор выделяемых веществ.
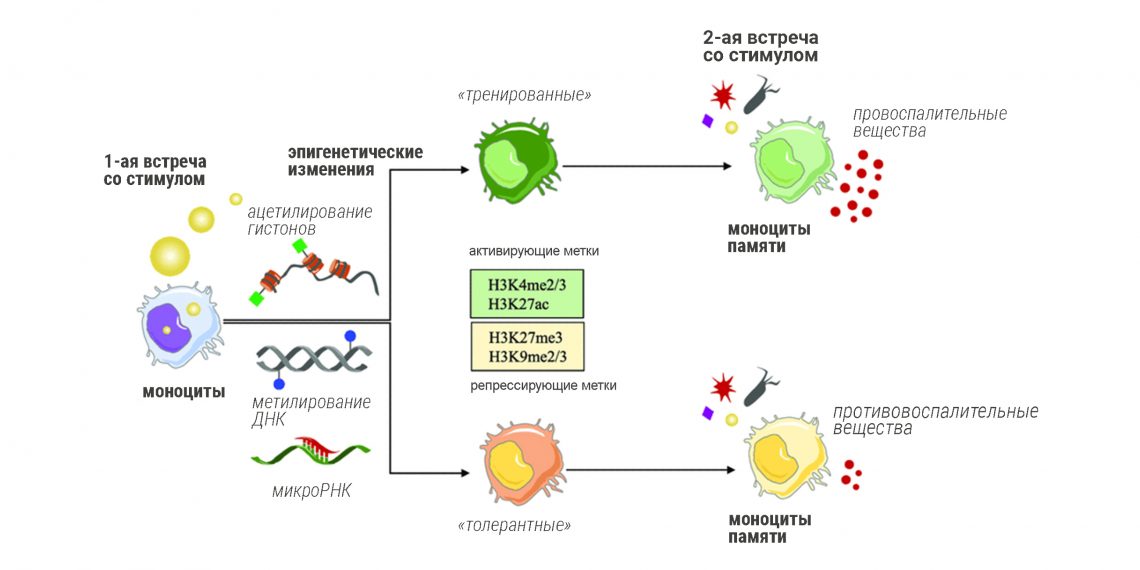
Судя по тому, что некоторые проявления иммунологической памяти сохраняются в течение месяцев или даже лет после первой «тренировки», изменения затрагивают не только взрослые клетки, но и стволовые, которые продолжают производить активированных предшественников. Тренируются даже «гражданские»: обитатели костного мозга и эпителиальных тканей после инфекции или прививки продолжают и дальше производить больше молекул, которые направляют перемещения иммунных солдат по организму — а от этого зависит, например, сколько их прибежит в лёгкое на борьбу с коронавирусом.
Мы не всегда можем до конца предсказать, возникнут ли эти изменения в случае каждой конкретной вакцины, а если и возникнут, то в какую сторону будут направлены.
Некоторые антигены‑раздражители вызывают толерантность иммунитета, то есть подавляют его работу. Другие же, наоборот, держат иммунную систему на взводе и позволяют ей агрессивнее реагировать на других врагов. В каких‑то случаях эти действия могут сочетаться: на одни раздражители натренированный иммунитет станет реагировать сильнее, на другие — слабее.
В каждом случае необходимо тщательно проверять, какую именно память оставляет после себя антиген. Иногда эти эффекты могут оказаться нам невыгодны — так, одна из вакцин от гриппа оказалась связанас аутоиммунной нарколепсией. А иногда «вакцинную тренировку» удаётся обратить на пользу людям. Например, БЦЖ подумывают использовать при рассеянном склерозе и уже испытывают как средство от диабета: вакцинация во младенчестве пользы здесь не приносит, а вот экстренное введение вакцины помогает приглушить аутоиммунную атаку организма на поджелудочную железу. Та же самая вакцина в других случаях оказывается полезна чтобы усилить иммунный ответ при раке мочевого пузыря, лейкемии, лимфоме и меланоме.
Теперь же у нас появилась возможность воспользоваться новооткрытым свойством врождённого иммунитета и обратить его «память» против вируса SARS‑CoV‑2. Рассчитывать на остатки от детской вакцинации едва ли имеет смысл — данные о том, насколько долго эффект тренировки после БЦЖ сохраняется в организме, сильно разнятся — от нескольких месяцев до десятков лет (хотя есть даже работа, в которой удалось проследить межпоколенческий эффект: дети реже умирали и лучше реагировали на прививку, если родились от вакцинированной матери). Зато можно заново привить взрослых людей и понадеяться на быструю защиту (но, возможно, кратковременную).
В этом случае, как и в истории с вакциной от полиомиелита, есть свои риски. Если иммунитет ответит на прививку слишком агрессивно, может возникнуть цитокиновый шторм, с которым организм не всегда способен справиться. Тем не менее в аналогичном исследовании, когда БЦЖ использовали против вируса жёлтой лихорадки, этого не произошло, и вакцина сработала успешно. Но в условиях эпидемии нельзя быть уверенным, что люди со слабым иммунитетом и старики адекватно отреагируют на вакцинацию. Поэтому, хотя клинические испытания БЦЖ как профилактики COVID‑19 уже начинаются по всему миру, от Дании до Австралии и Уганды, они будут ориентированы в первую очередь на медиков.
Таким образом, новый коронавирус здесь может выступить в качестве двигателя иммунологического прогресса. В условиях, когда от диабета или рака можно найти и другие лекарства, едва ли испытания профилактической вакцинации достигли бы такого размаха. Теперь же у нас есть шанс собрать большой объём данных о том, какими окольными путями могут действовать привычные нам вакцины, и проверить, так ли крепка наша врожденная иммунологическая память.
Источник: Лайфхакер





