Ученые из отдела биомедицинской инженерии университета Дьюка выяснили, что тренировка скелетных мышц человека способствует заживлению воспалительных процессов. Фокус исследования — влияние молекулярного мессенджера интерферона γ (IFN-γ), обычно повышенного при воспалительных процессах, на силу и структуру скелетных мышц человека.
Исследование описано в «Science Advances» в статье, озаглавленной «Имитирование упражнений и ингибирование JAK (Янус-киназы) снижают воздействие атрофии, вызванной IFN-γ, в искусственно созданных скелетных мышцах человека».
Более ранние исследования на людях и животных показали, что упражнения способствуют смягчению последствий воспаления, однако роль самих мышечных волокон в этом процессе не изучалась, равно как и их взаимодействие с молекулами, инициирующими процесс воспаления (например, IFN-γ).
По словам Ненада Бурсака (PhD, профессора биомедицинской инженерии в университете Дьюка), во время упражнений в организме человека происходит такое количество процессов, что трудно разобраться, какие функции выполняют отдельные системы и клетки. Он добавляет, что искусственно созданная исследователями система мышц является модульной, что подразумевает возможность сочетания в этой модели различных типов клеток и тканевых компонентов. Было выявлено, что мышечные клетки способны самостоятельно оказывать противовоспалительное действие.
Эти открытия были бы неосуществимы без разработки первой в своем роде исследовательской модели, которую специалисты в лаборатории Бурсака создавали почти десятилетие. Для имитации физических упражнений созданные в лаборатории мышечные волокна подвергались электрической стимуляции.
Кратковременное или острое воспаление — физиологическая реакция на инфекцию или повреждение, обычно сопровождающаяся покраснением, жаром и отеком, — представляет собой врожденный иммунный ответ, благодаря которому удаляются фрагменты отмерших клеток, а также происходит восстановление мышечной ткани. Однако когда иммунная система выходит из строя, воспалительная реакция может усилиться или продолжаться в течение длительного промежутка времени, что приводит к атрофии и повреждению окружающих тканей. Например, при таких заболеваниях, как ревматоидный артрит и саркопения, длительное неконтролируемое воспаление приводит к атрофии мышц.
Чжаовей Чен (PhD, научный сотрудник лаборатории Бурсака и первый автор статьи) заявляет, что хронические воспалительные заболевания приводят к атрофии мышц, однако до сих пор было неясно, произойдет ли аналогичное с образцами искусственно выращенных в чашке Петри человеческих мышц. Ученым удалось не только подтвердить, что IFN-γ в первую очередь работает по определенному сигнальному пути, но и показать, что стимуляция мышечных клеток с помощью упражнений может напрямую противодействовать этой провоспалительной сигнализации независимо от присутствия других типов клеток или тканей.
Исследователи из лаборатории Бурсака — первые, кому удалось вырастить скелетные мышцы человека в чашке Петри, обладающие почти полным функционалом естественной ткани (в том числе, способностью сокращаться). В лаборатории совершенствуют модель, добавляя в систему иммунные клетки и пулы стволовых клеток. Для настоящего исследования Бурсак и его команда исследователей подвергали эти выращенные в лаборатории мышцы воздействию высоких уровней IFN-γ в течение семи дней, чтобы имитировать эффекты длительного хронического воспаления. Как и ожидалось, мышца стала меньше и слабее.
Затем исследователи снова применили IFN-γ, но также провели электростимуляцию мышцы парой электродов, которые заставляли ее сокращаться, имитируя режим физических упражнений. Хотя ученые ожидали, что описанная выше процедура будет в некоторой степени способствовать росту мышц (как было выявлено в предыдущих исследованиях), они с удивлением обнаружили, что мышца вообще не стала меньше или слабее.
Авторы отмечают, что это первое исследование, в котором изучаются прямые и специфические эффекты IFN-γ на функционирование скелетных мышц человека. Впервые демонстрируется существование не зависящего от мышечных волокон противовоспалительного механизма (индуцируемого физическими упражнениями), в который вовлечены пути JAK/STAT1.
Помимо хорошо зарекомендовавших себя эффектов стимуляции роста и силы мышц, имитирующая упражнения электрическая стимуляция подавляла сигнальный путь JAK/STAT1 (от англ. signal transducer and activator of transcription 1 — преобразователь сигнала и активатор транскрипции 1), который обычно активируется посредством IFN-γ. Авторами показано, что два препарата, используемые для лечения ревматоидного артрита, тофацитиниб и барицитиниб, которые блокируют один и тот же путь, обладают одинаковым противовоспалительным действием.
По словам Бурсака, во время тренировки сами мышечные клетки напрямую
препятствовали провоспалительному сигналу, индуцированному IFN-γ, что
явно не ожидалось. Эти результаты показывают, насколько полезной для
открытия новых механизмов развития заболеваний и потенциальных методов
лечения может оказаться выращенная в лабораторных условиях скелетная
мышечная ткань. Существуют представления о том, что оптимальные уровни и
режимы физических нагрузок могут тормозить хроническое воспаление, не
нарушая гомеостаз отдельно взятых клеток. Возможно, искусственно
созданные скелетные мышцы человека могут помочь проверить, верны ли
такие представления.
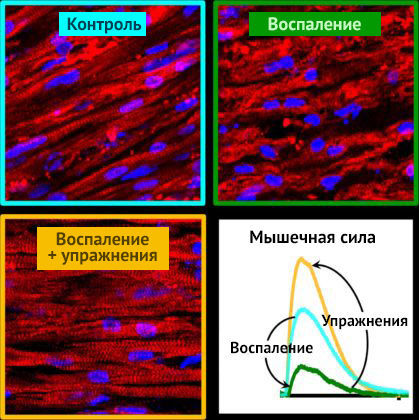
Рисунок 1 Длинные, тонкие, четко очерченные мышечные волокна (вверху слева) находятся в беспорядке после длительного воспаления (вверху справа), но сохраняют свою структуру (внизу слева) и силу (внизу справа) при тренировках во время воспаления (Чжаовей Чен, университет Дьюка).
Бурсак и его команда ожидают будущего использования своей модели мышечных волокон для изучения воспалительных заболеваний человека и противовоспалительных методов лечения.





