Ревматоидный артрит (РА) — хронический воспалительный артрит, характеризующийся аутоиммунным патогенезом, высоким уровнем коморбидности и высокой концентрацией антител. Развитие за последнее время продвинутой терапии, например синтетических ингибиторов янус-киназ (ИЯК/ JAKi) или биологических препаратов ингибиторов факторов некроза опухоли (иФНО/ TNFi).
Ключевыми факторами воспаления РА выступают В-лимфоциты, а потому очевидной идеей (судя по одобренному для терапии РА более 20 лет моноклональному антителу ритуксимабу) является их супрессия различными способами, и сейчас фармацевтическая промышленность занимается разработкой лекарств для полирезистентных или рефрактерных форм РА. Ограничением терапии ритуксимабом является низкая частота ремиссий (~30 %), потенциально связанная с особенностями всасывания и не совсем понятными случаями выживания CD20+ B-клеток и низкой деплецией (снижением численности) CD19+ плазмобластов, продуцирующих аутоантитела.
Для преодоления этой проблемы Bucci и соавт. попробовали использовать биспецифический активатор Т-лимфоцитов (BiTE) CD19-CD3, блинатумомаб, изначально применяемый при острой лимфобластной лейкемии. Молекула состоит из двух одноцепочечных вариабельных фрагментов (scFv) антител к CD3 и CD19, соединенных гибким линернымм участком. После связывания с CD3+ Т-лимфоцитами и CD19+ B-лимфоцитами блинатумомаб активирует направленное цитотоксическое уничтожение последних (Рис. 1).
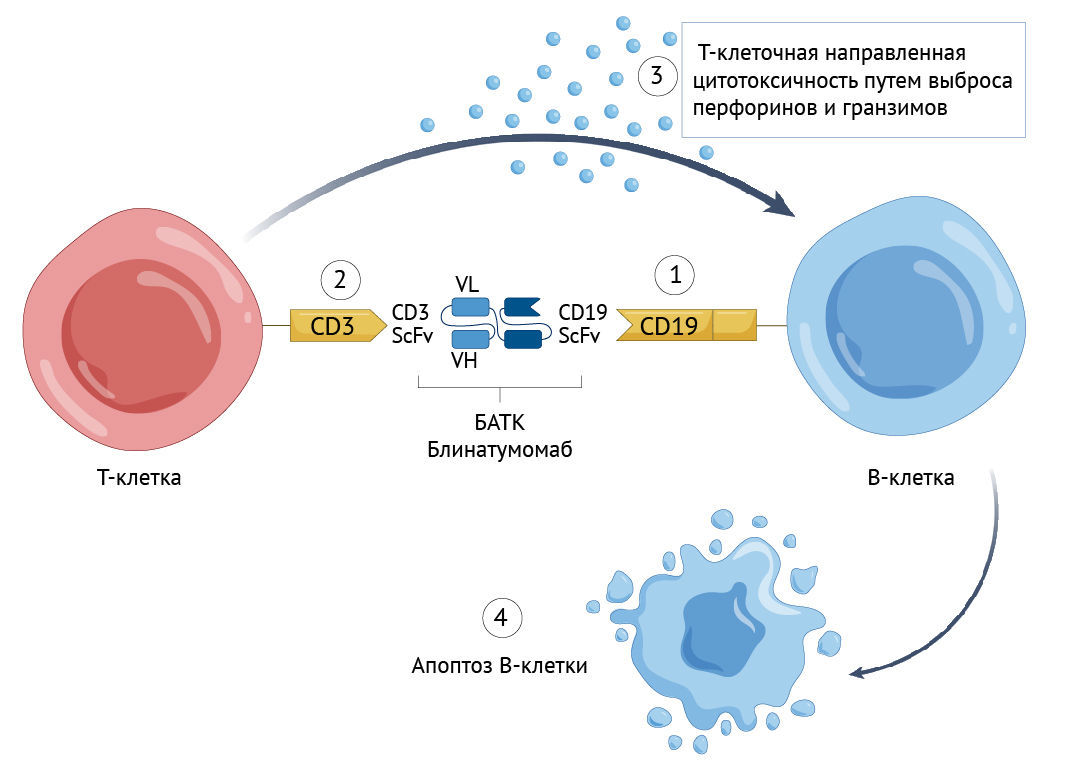
Рис. 1 | Механизм действия блинатумомаба.Начальное связывание scFv CD19 блинатумомабом (1), сопровождаемое связыванием scFv CD3 вызывает направленную Т-опосредованную цитотоксичность (3) и апоптоз гибель В-лимфоцитов (4). Аминокислотные последовательности VL и VH обозначают вариабельные легкие и тяжелые цепи, соответственно.
Авторы успешно применили терапию блинатумомабом у 6 пациентов с полирезистентным РА. У участников исследования было отмечено существенное снижение отека и болезненности суставов, а также объективных УЗИ-показателей синовита.
Несмотря на использование более низких доз блинатумомаба, чем при лейкемии, наблюдаемые результаты свидетельствуют о глубоком проникновении блинатумомаба в ткани у пациентов с РА: из 3-х пациентов, у которых получали образцы, у двух наблюдалось истощение пула синовиальных В-лимфоцитов,а у пациента, ранее получавшего лечение ритуксимабом (на момент исследования у него наблюдалось истощение B-лимфоцитов), был зафиксирован клинический ответ.
Клинический результат в основном сохранялся до 6 месяцев наблюдения, но у одного пациента, у которого сохранялись синовиальные CD20, вернулись симптомы, что подчеркивает необходимость оптимизации дозы. Кроме того, неожиданно был зарегистрирован ответ у пациента с РА, отрицательным по антителам к циклическому цитруллинированному пептиду и по ревматоидному фактору, так как обычно у серонегативных пациентов хуже ответ на ритуксимаб.
Важно, что за глубоким истощением B-лимфоцитов (включая B-клетки памяти) последовала репопуляция наивными, не переключающимися на другие классы B-клетками, что позволяет предположить, что блинатумомаб может привести к «перезагрузке» иммунного статуса пациентов с РА. В связи с этим было бы интересно специально изучить влияние блинатумомаба на IL-10-продуцирующие регуляторные В-клетки.
У пациентов с системной красной волчанкой CAR-T терапия оказывала схожее (с блинатумомабом) воздействие на популяцию B-лимфоцитов у пациентов, прошедших лечение, что дает заманчивую перспективу ремиссии или излечения без лекарств.
Однако у одного пациента (у которого была отложена поддерживающая терапия абатацептом) в описанной серии случаев произошло обострение болезни, что позволяет предположить необходимость больших доз для индукции длительной безлекарственной ремиссии.
Эти данные, безусловно, дают основания для будущих исследований блинатумомаба при РА и, возможно, при других В-клеточно-опосредованных аутоиммунных заболеваниях, таких как системная красная волчанка. Очень важно, чтобы протокол любого будущего исследования включал возможность глубокого клинического и биологического фенотипирования пациентов как до, так и после терапии, что позволит оптимизировать исходы для пациентов, получающих лечение блинатумомабом, и улучшить понимание патогенеза заболевания.





