В ходе пандемии, вызванной коронавирусом тяжелого острого респираторного синдрома 2 (SARS-CoV-2), клинические и научные сообщества и системы общественного здравоохранения были вынуждены реагировать на новые генетические варианты вируса. Каждый новый вариант вызвал шквал внимания со стороны средств массовой информации, различные реакции научного сообщества и призывы правительств либо «сохранять спокойствие», либо принять немедленные контрмеры. Хотя многие ученые первоначально скептически относились к значимости мутации D614G, появление нового «британского варианта» — линии B.1.1.7 — вызвало широкую озабоченность. Чтобы понять, какие именно варианты вызывают обеспокоенность и почему, необходимо разобраться в эволюции вируса и геномной эпидемиологии SARS-CoV-2.
Мутации, варианты и распространение
Мутации возникают как естественный побочный продукт репликации вирусов [1]. Частота мутаций у РНК-вирусов обычно выше, чем у ДНК-вирусов. Однако у коронавирусов происходит меньше мутаций, чем у большинства других РНК-вирусов, потому что они кодируют фермент, который исправляет некоторые ошибки, возникающие во время репликации. Как правило, судьба вновь возникшей мутации определяется естественным отбором. Частота тех мутаций, которые дают вирусу конкурентное преимущество в отношении репликации, распространения или ухода от иммунитета, будет увеличиваться, а те, которые снижают приспособленность вируса, склонны отбраковываться из популяции циркулирующих вирусов. Однако частота мутаций также может увеличиваться и уменьшаться в результате случайных событий. Например, «эффект основателя» возникает, когда в ходе распространения ограниченное число отдельных вирусов создает новую популяцию. Мутации, присутствующие в геномах этих вирусов-предков, будут доминировать в популяции независимо от их влияния на приспособленность. Такое же взаимодействие естественного отбора и случайных событий формирует эволюцию вируса внутри хозяев, в различных сообществах и странах.
Хотя термины «мутация», «вариант» и «штамм» при описании эпидемиологии SARS-CoV-2 часто используются как взаимозаменяемые, важно понимать различия между ними. Термин «мутация» относится к фактическому изменению последовательности (ДНК или белка): D614G обозначает замену аспарагиновой кислоты на глицин в положении 614 гликопротеина шиповидных отростков (S-белка). Геномы, последовательности которых различаются, часто называют вариантами. Этот термин несколько менее точен, поскольку два варианта вируса могут отличаться одной или несколькими мутациями. Строго говоря, вариант — это штамм, обладающий явно отличающимся фенотипом (например, различиями в антигенности, трансмиссивности или вирулентности).
Оценка нового варианта SARS-CoV-2 должна включать в себя ответы на следующие вопросы: достиг ли вариант доминирующего положения в результате естественного отбора или случайных событий? Если имеющиеся данные свидетельствуют о естественном отборе, то какие мутации подверглись отбору? Каково адаптивное преимущество этих мутаций? Какое влияние эти мутации оказывают на трансмиссивность и распространение, антигенность или вирулентность?
Мутация D614G S-белка
Мутация D614G гликопротеина шиповидных отростков (S-белка) SARS-CoV-2 была впервые обнаружена на значительном уровне в начале марта 2020 года и в течение следующего месяца достигла глобального доминирования [2]. По-видимому, изначально мутация возникла независимо и одновременно распространилась по нескольким географическим регионам. Эта очевидная конвергентная эволюция наводит на мысль о естественном отборе и адаптивном преимуществе D614G. Однако при последующих секвенированиях мутация D614G была выявлена в вирусах, которые были распространены в нескольких китайских провинциях в конце января. Это свидетельствует в пользу того, что глобальное распространение этой мутации могло быть результатом случайных событий с «эффектом основателя», когда вирусы, несущие 614G, просто инициировали большинство ранних случаев передачи в нескольких местах.
Такая правдоподобная нулевая гипотеза заставила многих в эволюционном сообществе усомниться, что мутация D614G была адаптивной, несмотря на данные, полученные in vitro, которые показывают ее влияние на связывание с рецепторами. Недавний популяционно-генетический и филодинамический анализ более 25 000 последовательностей из Великобритании показал, что вирусы, несущие 614G, по-видимому, действительно распространяются быстрее и дают начало более крупным филогенетическим кластерам, чем вирусы, несущие 614D [3]. Величина эффекта в данном анализе была умеренной, и различные модели не всегда достигали статистической значимости. Совсем недавно дополнительное исследование на животных показало, что вирусы, несущие 614G, передаются более эффективно [4, 5].
Мутация N453Y S-белка и норки
Тревожные вспышки SARS-CoV-2 начали происходить на норковых фермах в Нидерландах и Дании в конце весны и начале лета 2020 года [6]. Геномные и эпидемиологические исследования ранней вспышки в Нидерландах показали передачу вируса от человека к норке, от норки к норке и от норки к человеку [7]. В начале ноября 2020 года датские власти сообщили о 214 случаях заболевания человека коронавирусной инфекцией (COVID-19), связанных с норковыми фермами. Многие последовательности SARS-CoV-2 в Нидерландах и Дании несли мутацию Y453F в рецептор-связывающем домене S-белка, которая может усиливать его способность связываться с АПФ2 (ангиотензинпревращающим ферментом 2) у норок. У одиннадцати человек, заразившихся во время датской вспышки, обнаружен вариант вируса под названием «кластер 5», несущий в гене S-белка три дополнительные мутации (del69_70, I692V и M1229I). Первоначальное исследование девяти образцов сыворотки выздоравливающих людей показало умеренное и статистически значимое снижение нейтрализующей активности антител против вирусов из кластера 5 (в среднем в 3,58 раза; диапазон 0–13,5). Очевидная адаптация SARS-CoV-2 к норке, тем не менее, вызывает беспокойство, поскольку продолжающаяся эволюция вируса в организме животных-носителей потенциально может привести к повторным передачам нового SARS-CoV-2 от норки к человеку и другим млекопитающим. По этой причине многие страны активизировали усилия по эпиднадзору и в некоторых случаях осуществили крупномасштабные выбраковки (то есть выборочный забой) норок на фермах.
Линия B.1.1.7 и мутация N501Y
Линия B.1.1.7 (также называемая 501Y.V1) представляет собой филогенетический кластер, который быстро распространяется на юго-востоке Англии [8] (Рисунок). До его обнаружения в начале сентября эта линия накопила 17 специфических мутаций, что свидетельствует о значительной предшествующей эволюции, возможно, в хронически инфицированном хозяине. По состоянию на 28 декабря 2020 года на этот вариант приходилось примерно 28 % случаев заражения SARS-CoV-2 в Англии, и популяционно-генетические модели позволяют предположить, что данная линия распространяется на 56 % быстрее других. В отличие от D614G, для которой, вероятно, могли быть выгодными ранние случайные события, линия B.1.1.7 распространилась, когда SARS-CoV-2 выявлялся уже повсеместно, и, по-видимому, достигла доминирующего положения, превзойдя существующую популяцию циркулирующих вариантов. Это убедительно говорит о естественном отборе вируса с большей трансмиссивностью на популяционном уровне. В то время как меры общественного здравоохранения, такие как маски, соблюдение дистанции и ограничение больших скоплений людей, должны оставаться эффективными, но борьба с более трансмиссивным («более заразным») вариантом, вероятно, потребует более строгого применения и повсеместного принятия этих мер.
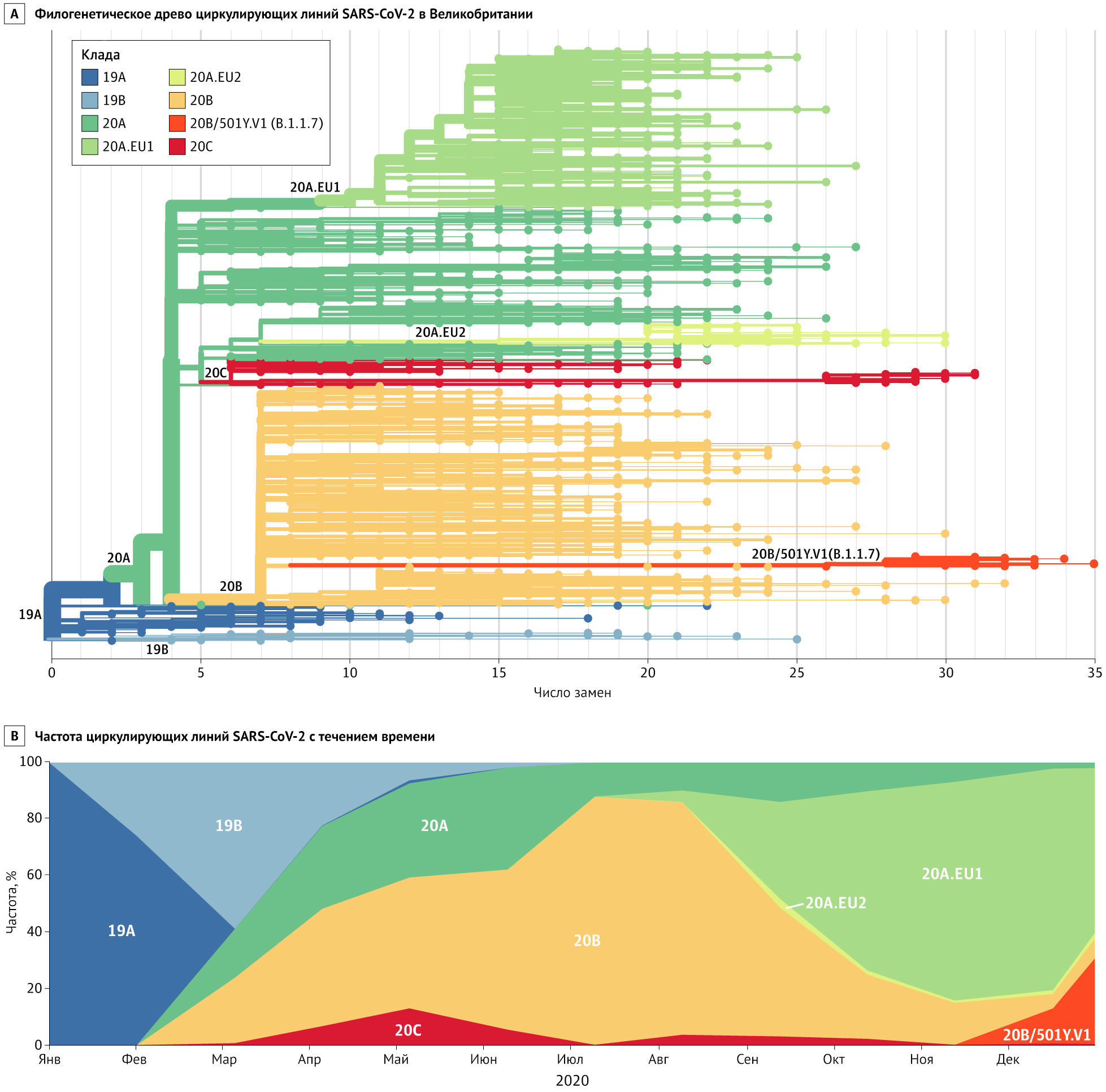
Распространение нового варианта SARS-CoV-2А. Филогенетическое древо, показывающее связь линии B.1.1.7 (20B/501Y.V1, оранжевые линии и точки) с другими циркулирующими линиями. Большая длина ветви для этой линии отражает тот факт, что она накопила значительное число мутаций до того, как была обнаружена.
В. Частота циркулирующих линий с течением времени. Линии окрашены так же, как и на дереве, т.е. линия B.1.1.7 (20B/501Y.V1) показана оранжевым цветом.
Восемь мутаций линии B.1.1.7 затрагивают гликопротеин шиповидных отростков (S-белок), в числе которых N501Y в рецептор-связывающем домене, делеция 69_70 и P681H в сайте расщепления фурином. Все эти мутации могут влиять на связывание АПФ2 и репликацию вируса. Предполагается, что варианты с заменой 501Y в S-белке обладают более высоким сродством к АПФ2 человека. Другой вариант, также с мутацией N501Y, быстро распространяется в Южной Африке. Влияние этих мутаций на антигенность в настоящее время не ясно.
Иммуногенность и эффективность вакцины
Наблюдение за вариантами SARS-CoV-2 в основном сосредоточено на мутациях в гликопротеине шиповидных отростков (S-белке), который опосредует прикрепление к клеткам и является основной мишенью нейтрализующих антител. Существует большой интерес к тому, способствуют ли мутации в S-белке ускользанию от антител хозяина и могут ли они потенциально поставить под угрозу эффективность вакцин, поскольку в современных вакцинах именно S-белок является основным вирусным антигеном. На данном этапе строгий отбор вариантов на уровне популяции, вероятно, не обусловлен антителами хозяина, поскольку на данный момент нет достаточного количества иммунных индивидов для систематического продвижения эволюции вируса в каком-либо определенном направлении. Напротив, если у варианта в S-белке есть одна или несколько мутаций, повышающих трансмиссивность, он может быстро превзойти и вытеснить другие циркулирующие варианты. Поскольку современные вакцины вызывают иммунный ответ на весь S-белок, все еще есть надежда на эффективную защиту, несмотря на некоторые изменения в антигенных участках у различных вариантов SARS-CoV-2.
Разделение причины и следствия важно при оценке данных по нейтрализации антителами вариантов S-белка. Независимо от причины отбора мутации, разумно ожидать, что многие мутации в S-белке могут повлиять на нейтрализацию антителами. Поэтому важно учитывать как уровень изменения нейтрализации, так и количество проанализированных образцов сыворотки. Другая проблема заключается в том, что вирусные гликопротеины подвержены эволюционным компромиссам. Иногда мутация, усиливающая одно свойство вируса, например, связывание с рецептором, может ослабить другое свойство, такое как избегание антител хозяина. Действительно, недавние данные указывают на то, что это может иметь место в случае D614G [10]. Возможно, что мутации в S-белке, которые «полезны» для вируса прямо сейчас, также могут сделать его менее приспособленным к преодолению популяционного иммунитета в будущем. Определение этой динамики и ее потенциального влияния на эффективность вакцин потребует широкомасштабного мониторинга эволюции SARS-CoV-2 и иммунитета хозяина в течение длительного времени.





